不安障害は,恐怖・不安感情の制御障害を基盤とする疾患であり,30%程度の生涯有病率が報告されている.多くの不安障害は不眠を高率に合併し,50~90%の患者が何らかの不眠を訴える.恐怖・不安は不眠の慢性化における重大な促進・遷延因子であり,両病態は密接に関連し,不安障害患者は不眠の素地を備えた集団であるといえる.長年,不安障害治療の中心的役割を担っていたbenzodiazepine系薬剤は,不眠症に対しても有効であり,最高血中濃度到達時間や血中濃度半減期の長さにより,抗不安薬と睡眠薬との使い分けがされているにすぎず,これも病態共通性を支持する根拠となる.不眠症は,不安対象が不眠自体もしくは不眠により生じると予期される心身の不調に限定された“不安障害”と考えることもできる.実際,不眠症患者の日中の機能障害には,不安症状もしくは心気症状と考えうるものも多く,不安障害の潜在的な合併は極めて多いと推測される.近年,不安障害の治療はSSRIsやSNRIsなどの抗うつ薬や認知行動療法にシフトし,国際的な治療ガイドラインにおいても優先順位の高い治療法とされている.しかし病態特性から考えると,不安障害に合併した不眠の治療は不安障害の治療と同時に行われるべきであり,独立した病態として治療すると過剰医療に陥る可能性も孕んでいる.
2)国立大学法人滋賀医科大学精神医学講座
はじめに
不安障害は,恐怖・不安感情の制御障害を基盤とする疾患であり,30%程度の生涯有病率が報告されている4).不安障害はうつ病と並び,不眠を合併するリスクが極めて高い疾患であるが,不安障害のなかでも全般不安症(generalized anxiety disorder:GAD)は特に不眠の合併が多い.GADはうつ病と連続性を有する病態であると考えられているが,他方で不眠症との病態共通性も高いと推測される.
本稿では,うつ病-GAD-不眠症という病態スペクトラムのなかで,GADに合併する不眠をいかに治療するべきか考察する.恐怖・不安はGADの中核病態であるとともに,不眠の慢性化における重大な促進・遷延因子である.GADと不眠は密接に関連した病態であり,GAD患者は不眠の素地を備えた集団であるといえる.長年,不安障害治療の中心的役割を担っていたbenzodiazepine(BZD)系薬剤は,不眠症に対しても有効であることはこれを支持する重要な傍証である.しかし,近年の国際的な共通理解では,GADは選択的セロトニン再取り込み阻害薬(selective serotonin reuptake inhibitors:SSRIs)やセロトニン・ノルアドレナリン再取り込み阻害薬(serotonin and norepinephrine reuptake inhibitors:SNRIs)などの抗うつ薬や認知行動療法(cognitive behavioral therapy:CBT)を主体に治療すべきであり,BZD系薬剤の使用は限定的とされている.しかしこれらの治療法を用いると,合併する不眠に対しては異なる治療オプションを併用せざるを得ない事態も生じうる.不安障害に合併した不眠の治療は不安障害の治療と同時並行的に行われるべきであり,独立した病態として治療すると過剰医療に陥る可能性もある.本稿では不安障害と不眠病態の関連性および治療法に関し,現状と今後工夫すべき点に関して考察する.
I.不安障害
米国精神医学会による精神障害の診断と統計マニュアル第5版(Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition:DSM-5)では,不安障害群は発達の観点を含めて好発年齢順に7つの下位診断(分離不安症,選択性緘黙,限局性恐怖症,社交不安症,パニック症,広場恐怖症,全般不安症)で構成されている2).不安障害は過剰な恐怖・不安を特徴とする疾患群であり,情動処理に係る高次神経処理回路の成熟度合と,成長に伴う社会的役割・環境の変化が発症に影響する.各下位診断はこうした背景をもとに好発年齢が低い順に列記されているが,同時に社会機能障害を基準とした重症度の低い順とも考えられる.
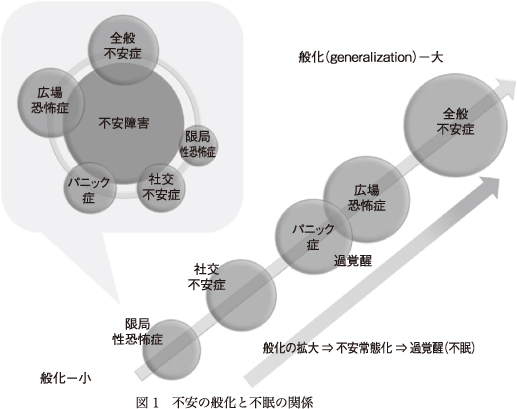
恐怖は,実在する既知の特定の対象もしくは普遍的な脅威に対する心理・生理的反応であるのに対し,不安は未来的予測に基づく,未知の漠然とした対象もしくは葛藤に対する反応である.恐怖の対象はしばしば発達段階に応じ変化するが,対象が増加することはまれであるのに対し,不安は容易に拡大し対象が増加しうる.これは不安が漠然とした将来起こりうる物・事に対する情動反応であるため,不安が強まると般化(generalization)し,不安範囲が拡大し,不安対象が増加する傾向があるためである.恐怖・不安の強度とその対象が増加・拡大するに伴い,緊張,過覚醒,回避行動が重症化し社会生活を送るうえで障害となる(図1).回避行動により恐怖・不安強度が軽減されることがあるが,多くの場合一時的役割しか果たさず社会機能障害はかえって悪化することも多い.
過覚醒症状の重症化に伴い不眠が合併しやすくなる.GADは不安の般化が拡大し,多数の対象に過剰な不安を抱く病態であり,不安障害のなかでも社会機能障害が高度化しやすい.不安障害のなかでDSM-5の診断基準に睡眠障害(入眠・睡眠維持困難,もしくは熟眠障害)が含まれるものはGADのみであり,病態を反映しているといえる.
II.不眠症における不安・恐怖病態
睡眠-覚醒プロセスは,覚醒時間の長さや日中の労作量に比例して高まる眠気(疲労)要因を解消する「ホメオスタシス」機構と,視床下部視交叉上核に中枢をもつ概日時計により約24時間の周期で発振する「概日リズム」機構の2システムで制御されると考えられている.多くの精神疾患に睡眠障害が高頻度で合併し,大規模災害などの重大なストレスイベント直後に不眠を呈する者が急増することから,近年は「情動制御」機構という第3のシステムによる睡眠-覚醒制御への関与が注目されている3).不眠症の中核的病態を示す精神生理性不眠においては,睡眠妨害学習の形成や不眠自体への恐怖といった,情動処理不全の病理が特徴であることも,睡眠障害と恐怖・不安との関連の強さを裏づけている10).
睡眠妨害学習とは睡眠環境と恐怖・不安感情の連合学習が形成されることを示す.多くの不眠症患者は,就寝時刻が近づくたびに「今日も眠れないのではないか」という不安に苛まれる.これにより寝室に入る,もしくはベッドに横たわると恐怖感情が自動的に惹起されるようになり,直前まで眠気を感じていたにもかかわらず,床に入るとかえって覚醒度が高まる.これは恐怖条件づけと呼ばれる,学習により獲得される生理的反応で説明づけられ,床のなかで「頑張って」眠りにつこうともがけばもがくほど,覚醒度が高まるという悪循環に陥る22).さらに,不眠症患者は夜に十分眠れないと,翌日の日中にひどい倦怠感や眠気に襲われ,すべき仕事・日課や趣味の活動でさえもこなすことができないと思い込み,強い不安を覚える.一部の不眠症患者においては,重篤で致死的な疾患に罹患する不安に苛まれる.こうした心理状況は不安症や近縁疾患とされる身体症状症・病気不安症と酷似しており,修正困難な思い込みに基づく予期不安と考えられる.
さらに,睡眠薬を長期使用している不眠症患者の心理特性において,「睡眠薬使用状況」への不安が指摘されている.「睡眠薬を飲めば眠れるが,毎日服用していて大丈夫なのだろうか」といった不安を抱えている患者は少なくない.特に近年,BZD系睡眠薬の長期連用に関する社会的疑念が国際的に高まっており,報道などで流布される状況下でこうした心理的ジレンマを抱きやすくなっている.睡眠薬常用に対する不安は覚醒度を高める要因となり,睡眠薬による覚醒度低下効果と拮抗し,「睡眠薬を飲んでいるのに眠れなくなってきた」というアンビバレントな状況を招く可能性がある.こうした状況は,「不眠がさらに悪化したのではないか」「頼みの綱である睡眠薬が効かなくなってきた」という絶望的な認知を惹起する.その結果,可能な限り減量・中止したいはずの睡眠薬を増量せざるを得ない事態に発展し,睡眠薬に「耐性」が形成されてしまったと思い込み,不安が増幅する悪循環に陥っている場合も少なからず見受けられる.
これらのように,慢性不眠症の成立にはさまざまな不眠の促進・遷延因子が関与しており,その中核は情動処理不全に基づく過覚醒であることが推測される19).
III.不安障害に合併する不眠の特徴
前述のように,不安障害のなかでもGADは診断基準に不眠症状を含んでおり,不眠症との病態共通性が高い疾患である3).実際,これらの疾患の治療は併存する睡眠障害の改善を同時にもたらし,また不眠症状にのみ焦点化した認知行動療法(cognitive behavioral therapy for insomnia:CBT-I)がGADの症状改善をもたらす,双方向的な関係性が示されている1)9).
GADは不特定多数の対象への過度で制御困難な慢性不安を特徴とする疾患である.多くは他の不安障害の診断基準を満たす病態を併存していることから,不安の般化がGADの中核病態であると考えられる.GADの患者は精神的苦痛にとどまらず心身症的症状を随伴することも多く,特に成人においては不眠をはじめとし,休息感のなさ,易疲労性,集中力低下,落ち着きのなさ,筋肉の過緊張といった身体的症状が高頻度に随伴することが診断基準に含まれる.
GADの病態仮説として,ストレス応答系である視床下部-下垂体-副腎皮質(hypothalamic-pituitary-adrenal:HPA)系や交感神経系の機能障害が推測されている12).脳機能画像研究によると情動調節系である前頭葉-前帯状皮質-扁桃体ネットワークにおいて,前頭葉・前帯状皮質の活動低下および扁桃体の過活動が報告されており13),前頭葉による情動のトップダウン制御障害が過剰な不安発現や不安対象の拡大をもたらしていると考えられている.こうした神経内分泌病態や脳機能病態は慢性不眠症の患者でも極めて類似した結果が報告されている21).
GAD患者の60~70%が何らかの不眠を訴え,入眠困難や睡眠維持困難(中途覚醒・早朝覚醒),熟眠感欠如,日中の眠気など,症状は多彩である1).さらに,GADの不安重症度と不眠症状の重症度に相関関係が認められることから,不眠はGADの中核症状の1つであると推測されている.うつ病も不眠の合併率が高い疾患であるが,うつ病は不眠が先行して出現する率が4割超であるのに対して,不安障害は2割弱であり,むしろ不安症状と同期して不眠が発生する率が4割近いことから不安と不眠の強い病態関連性がうかがえる9).また,GAD患者ではrapid eye movement(REM)睡眠関連随伴症である悪夢と睡眠麻痺の有症率が一般人口の約3倍と有意に高いことが近年のメタ解析研究で報告されている18).これらの睡眠随伴症は,抗ストレスホルモンであるコルチゾルの分泌上昇および,HPA系の過活動との関連が示唆されており,病態関連性の高さを裏づけている.GAD患者の睡眠構造に関して,健常者と比較した睡眠ポリグラフ(polysomnography:PSG)研究では,総睡眠時間の短縮,睡眠効率の低下,中途覚醒の増加,Stage 2睡眠時間の短縮,Stage 4睡眠潜時の延長が報告されている20).しかし,これらの睡眠構造上の特徴は,原発性の不眠症と極めて類似しており疾患特異性はないと考えられる.さらにGADは,慢性ストレスが発症因もしくは準備因子となるうつ病やアルコール使用障害などを高率に合併し,これらの疾患も不眠を高率に合併することから8),不眠の病態は複雑となりがちである.
IV.不安障害に合併する不眠の治療戦略
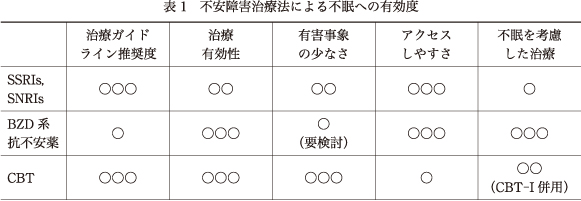
生物学的精神医学会世界連合(World Federation of Societies of Biological Psychiatry:WFSBP)による治療ガイドライン5)では,GADの薬物療法において,SSRIsやSNRIs,そして本邦では疾患適応は未承認のpregabalinを第一選択薬として推奨している.CBTは上記薬物療法と並んで推奨する治療法であるが,国や社会的状況により薬物療法に比べてアクセスのしやすさに差が大きいため,患者が希望し,医療供給条件が整っている場合にのみ選択される治療法と位置づけられている.さらに,上記薬物療法やCBTが無効であった場合には,短期的な使用を前提としてBZD系抗不安薬の使用を推奨している(表1).
GADに対する治療有効性を検討したメタ解析研究によると,SSRIsを含む抗うつ薬はGADの改善に一定の有効性を示すことが報告されている11).同研究ではCBTの有効性も同様に示されているが,CBTによる有効性の強さを示す効果量は抗うつ薬よりも高いことが示唆されている.さらにBZD系抗不安薬の有効性はCBTに匹敵し,抗うつ薬よりも高いことが示されている.
BZD系抗不安薬は抗不安効果とともに催眠効果を有するため,不眠を合併するGADの治療薬としては合理的な治療法である可能性がある.しかし他方で,依存性などの有害事象を鑑みた国際的なBZD処方抑制の流れを受けて,ガイドラインによる推奨度は下げられている.BZD系抗不安薬は抗うつ薬よりも離脱が少なく,アドヒアランスが良好であり(RR=0.40,95% CI=0.20~0.57),さらに副作用の発現も抗うつ薬より少ないことが示されている(RR=0.41,95% CI=0.34~0.50)14).
GADに対するCBTは不安症状を改善させるのみならず,不眠症状を改善することが示唆されている(ES=0.527,95% CI=0.306~0.748)7).さらに,SSRIsに分類される抗うつ薬であるsertralineは,GADに併存する不眠の改善にも有効であることが報告されている1)5)7).これに対して,不眠を治療ターゲットにした認知行動療法であるCBT-IをGAD合併不眠に用いることで,不眠を改善させるのみならず不安症状に対しても有意な治療効果があることが報告されている6).これらの知見はGADと不眠の病態共通性を支持する傍証であり,両症候に対しては複合的・同時的な治療戦略をとる必要性を示唆している13).実際,SSRIsであるescitalopramに非BZD系睡眠薬であるeszopicloneを併用した場合,escitalopram単剤(プラセボ同時投与)治療と比較してGAD重症度および不眠症状以外の不安関連症状の改善率が高く,eszopiclone投与中止後も有意に改善効果が持続することが報告されている16).
おわりに
GADはしばしば慢性経過をとり,長期にわたり患者のQOL(quality of life)を低下させる疾患である15).またGADは能力障害や社会機能障害も生じるため,医療経済への負担のみならず経済損失への影響も無視できない12)17).他方で不眠も慢性化すると患者のQOLを低下させ長期的な医療が必要となることが多く,両者の合併を適切に治療することが重要である.GADをはじめとする不安障害では併存する不眠との病態共通性が高く,各々の症状が症状促進的な交互作用を示すため,共通病態に有効な治療法は,両者を一元的に治療できる可能性が期待できる.現在GADの薬物療法において優先的に推奨されているSSRIs・SNRIsは合併不眠の治療には効果が不十分である可能性もあり,この場合その他の不眠治療薬の併用も臨床的には有用となる可能性があるが,ポリファーマシーに陥る危険性もあり慎重な投薬デザインが必要である.CBTはGADの治療において有効性が高く有害事象も少ない重要な治療オプションであり,CBT-Iコンポーネントを組み合わせることで不安と不眠を一元的に治療できる可能性が高い.しかし,本邦ではCBTの実施可能な施設が限られていることもあり早急な診療・社会保障システムの整備が望まれる.BZD系薬剤の適切な使用は,GAD症状の緩和とともに不眠の治療にも貢献するが,長期使用に伴う有害性が懸念されており,限定的な使用にとどめざるを得ない.長期的な転帰を含め,GAD患者のQOLおよびADL(activities of daily living)改善に,抗うつ薬,BZD系薬剤,CBTがどのように寄与するのか,多角的な調査・検討が必要とされる.
GAD患者の発症脆弱性背景も含めると,臨床家は治療法選択にできうる限り多くのオプションを必要としている.GADは不安閾値の極めて低い集団であることから,臨床家は提供する治療法の弱点を適切に理解し説明することができないと,GAD患者に新たな不安要素を与えることにもつながり治療が難渋することも考えうる.このため,患者の長期的転帰を多角的に考慮した臨床研究が早急に求められている.
なお,本論文に関連して開示すべき利益相反はない.
1) Alvaro, P. K., Roberts, R. M., Harris, J. K.: A systematic review assessing bidirectionality between sleep disturbances, anxiety, and depression. Sleep, 36; 1059-1068, 2013![]()
2) American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders, 5th ed (DSM-5). American Psychiatric Publishing, Arlington, 2013 (日本精神神経学会 日本語版用語監修, 髙橋三郎, 大野 裕監訳: DSM-5精神疾患の診断・統計マニュアル. 医学書院, 東京, 2014)
3) Baglioni, C., Spiegelhalder, K., Lombardo, C., et al.: Sleep and emotions: a focus on insomnia. Sleep Med Rev, 14; 227-238, 2010![]()
4) Bandelow, B., Michaelis, S.: Epidemiology of anxiety disorders in the 21st century. Dialogues Clin Neurosci, 17; 327-335, 2015![]()
5) Bandelow, B., Sher, L., Bunevicius, R., et al.: Guidelines for the pharmacological treatment of anxiety disorders, obsessive-compulsive disorder and posttraumatic stress disorder in primary care. Int J Psychiatry Clin Pract, 16; 77-84, 2012![]()
6) Belleville, G., Cousineau, H., Levrier, K., et al.: Meta-analytic review of the impact of cognitive-behavior therapy for insomnia on concomitant anxiety. Clin Psychol Rev, 31; 638-652, 2011![]()
7) Belleville, G., Cousineau, H., Levrier, K., et al.: The impact of cognitive-behavior therapy for anxiety disorders on concomitant sleep disturbances: a meta-analysis. J Anxiety Disord, 24; 379-386, 2010![]()
8) Caporino, N. E., Read, K. L., Shiffrin, N., et al.: Sleep-related problems and the effects of anxiety treatment in children and adolescents. J Clin Child Adolesc Psychol, 46; 675-685, 2017![]()
9) Craske, M. G., Stein, M. B., Eley, T. C., et al.: Anxiety disorders. Nat Rev Dis Primers, 3; 17024, 2017![]()
10) Dolsen, M. R., Asarnow, L. D., Harvey, A. G.: Insomnia as a transdiagnostic process in psychiatric disorders. Curr Psychiatry Rep, 16; 471, 2014![]()
11) Gonçalves, D. C., Byrne, G. J.: Interventions for generalized anxiety disorder in older adults: systematic review and meta-analysis. J Anxiety Disord, 26; 1-11, 2012![]()
12) Mochcovitch, M. D., da Rocha Freire, R. C., Garcia, R. F., et al.: A systematic review of fMRI studies in generalized anxiety disorder: evaluating its neural and cognitive basis. J Affect Disord, 167; 336-342, 2014![]()
13) O'Byrne, J. N., Berman, R. M., Gouin, J. P., et al.: Neuroimaging findings in primary insomnia. Pathol Biol (Paris), 62; 262-269, 2014![]()
14) Offidani, E., Guidi, J., Tomba, E., et al.: Efficacy and tolerability of benzodiazepines versus antidepressants in anxiety disorders: a systematic review and meta-analysis. Psychother Psychosom, 82; 355-362, 2013![]()
15) Olatunji, B. O., Cisler, J. M., Tolin, D. F.: Quality of life in the anxiety disorders: a meta-analytic review. Clin Psychol Rev, 27; 572-581, 2007![]()
16) Pollack, M., Kinrys, G., Krystal, A., et al.: Eszopiclone coadministered with escitalopram in patients with insomnia and comorbid generalized anxiety disorder. Arch Gen Psychiatry, 65; 551-562, 2008![]()
17) Sado, M., Takechi, S., Inagaki, A., et al.: Cost of anxiety disorders in Japan in 2008: a prevalence-based approach. BMC Psychiatry, 13; 338, 2013![]()
18) Saletu, B., Anderer, P., Saletu-Zyhlarz, G. M.: Recent advances in sleep research. Psychiatr Danub, 25 (4); 426-434, 2013![]()
19) Spielman, A. J., Nunes, J., Glovinsky, P. B.: Insomnia. Neurol Clin, 14; 513-543, 1996![]()
20) Stein, M. B., Sareen, J.: Clinical practice generalized anxiety disorder. N Engl J Med, 373; 2059-2068, 2015![]()
21) Waters, F., Moretto, U., Dang-Vu, T. T.: Psychiatric illness and parasomnias: a systematic review. Curr Psychiatry Rep, 19; 37, 2017![]()
22) Yoshiike, T., Kuriyama, K., Honma, M., et al.: Neuroticism relates to daytime wakefulness and sleep devaluation via high neurophysiological efficiency in the bilateral prefrontal cortex: a preliminary study. Psychophysiology, 51; 396-406, 2014![]()