アルツハイマー病を中心とした認知症患者は時に易怒性や興奮,妄想を呈し,これらはbehavioral and psychological symptoms of dementia(BPSD)と呼ばれ臨床現場で問題となる.これまではBPSDが強く対応が困難な場合には抗精神病薬が用いられることが多かった.しかしながら2005年の米国のメタアナリシスで,非定型抗精神病薬を投与した群の死亡率が1.6~1.7倍高まると報告され,FDAが警告を出した.2016年のAPAガイドラインではリスクとベネフィットを十分に考慮した後に使用するよう述べられている.本邦では認知症患者への抗精神病薬投与に関して保険適用上の問題はあるが強い規制はない.本邦における使用推移の報告では,定型抗精神病薬の使用量は減少しているが非定型抗精神病薬の使用量は増加している.本邦の大規模コホート研究では,抗精神病薬を新規投与された群で11週以降の死亡リスクが約2.5倍上昇したと報告された.そのため2017年の認知症疾患診療ガイドラインにおいても,BPSDに対して非薬物的な介入を行うことが優先されるとされている.まず薬物療法の前に非薬物的な介入を,というのがコンセンサスと考えられる一方で,BPSDに十分なエビデンスのある非薬物療法があるわけではない.逆説的ではあるが,定型的な薬物療法に行き詰まったときこそ,問題となる症候を再検討し,診断を再考し,その他BPSDに影響を与える身体状況や心理社会的要因などを検討することが重要となる.著者らはBPSDへの治療の新しい取り組みもいくつか行っている.BPSDの抗精神病薬治療への反応予測因子がわかれば,抗精神病薬が有効かどうか治療前に判断することが可能となる.さらにBPSDへの非薬物的な介入の集合知収集のための試みも行っている.これらの取り組みは将来のBPSDの予防・治療において重要である.
はじめに
認知症患者では経過のなかで易怒性,興奮,妄想,昼夜逆転といった行動・心理症状(behavioral and psychological symptoms of dementia:BPSD)が出現する.これらの症状は患者の生活の質を低下させ,介護者の介護負担を増し,早期からの入院・施設入所の原因ともなる重要な症状であり,臨床場面においては精神科医が対処を求められることが多い.特に易怒性や興奮といったBPSDに対しては緊急性のある対応が求められることが多く,そのようなBPSDに対する薬物療法として,これまで抗精神病薬が使用されることが多かった.実臨床においては特に錐体外路症状などの副作用が比較的少ない非定型抗精神病薬が用いられやすい傾向にある.本間が2000年代に行った使用実態に関するアンケート調査では,精神科専門病院に勤務する精神科医で診ている認知症患者の62%にBPSDが認められ,そのうち93%が薬物療法を受け,そのうち81%が抗精神病薬を使用しているという状況であった5).
I.抗精神病薬の使用への警鐘
そのような状況のなかで,そもそも認知症のBPSDに対してはたして抗精神病薬が有効なのかという疑問がある.北米で行われた,CATIE―ADという大規模な非定型抗精神病薬の二重盲検プラセボ対照試験は,精神症状を伴うアルツハイマー病(Alzheimer’s disease:AD)421例にオランザピン,クエチアピン,リスペリドン,プラセボを割り付けし,用量は随時調整し36週間の観察を行うというデザインで行われた.観察中に薬物が中断になる例が多く,結果として,副作用はAD患者の精神病症状,攻撃性,または激越に対する非定型抗精神病薬の利点を相殺すると結論づけている18).
同時期の2005年に15の無作為盲検試験のメタアナリシスが発表され,非定型抗精病神薬はプラセボに比べ1.6~1.7倍死亡リスクを高めると報告された17).それを受け,米国食品医薬品局(Food and Drug Administration:FDA)が同年にオランザピン,クエチアピン,リスペリドンなどの非定型抗精神病薬を高齢者に投与した場合の危険性を警告した.しかし定型抗精神病薬には警告がなかったことから,非定型抗精神病薬と定型抗精神病薬を比べる報告もなされ,高齢者の死亡率は非定型抗精神病薬よりも定型抗精神病薬のほうが高かったと報告された19).これを受け,FDAから2008年に定型抗精神病薬にも同様の警告がなされることになった.
2014年の16の二重盲検プラセボ対照試験のメタアナリシスでは,抗精神病薬群3,343例とプラセボ群1,707例を評価し,非定型抗精神病薬はBPRS,CMAI,NPI,CGI-C,CGI-Sといった評価尺度のすべてでプラセボと比較して有効であったものの,傾眠〔odds ratio:(OR)=2.95〕,錐体外路症状(1.74),脳血管障害(2.50),尿路感染症(1.35),浮腫(1.80),歩行障害(3.35),死亡(1.52)は高頻度であり,有効性,安全性および忍容性は,臨床的に注意深く考慮されるべきであると結論づけられている9).
一方で,定型抗精神病薬(n=138),非定型抗精神病薬(n=95)を使用したナーシングホーム利用者の縦断追跡では,死亡率の差に関して,種々の交絡因子(特に精神症状の強さ)の影響を除外すると抗精神病薬の影響は消失すると報告された.このような異なる結果の報告もあることを付記しておく8).
いずれにせよ,これらの報告により,認知症患者のBPSDに対して抗精神病薬は以前に比べて用いづらい状況となった.米国精神医学会(American Psychiatric Association:APA)の認知症患者への抗精神病薬投与の2016年ガイドラインにおいては,①緊急性が低い例への抗精神病薬治療は,焦燥および精神症状が重度,危険,著しい苦痛の原因となる場合のみ,②先行して,非薬物療法が有効かどうかを十分検討する,③治療前に,潜在的なベネフィットとリスクを評価して患者や代諾者と相談する,④低用量で開始し,最小有効用量になるまで漸増していく,⑤副作用があった場合,リスクとベネフィットを検討したうえで薬剤を中止すべきかを判断する,⑥治療開始から4週間たっても効果がみられない場合は,漸減の後に中止する,⑦十分な効果が得られた場合,開始から4ヵ月以内に漸減や中止を試みる,⑧投与中止後月1回以上の経過観察を少なくとも4ヵ月続ける,などの内容が述べられている16).
II.本邦での変化
このような流れを受けて,本邦での認知症患者のBPSDに対して抗精神病薬使用はどのように変わったのであろうか? Okumura, Y.らはレセプトを無作為抽出した社会医療診療行為別調査のデータの二次解析において認知症高齢者に対する抗精神病薬の使用の縦断的変化の調査を行った.2008~2010年に抗精神病薬は全体の21.3%に用いられており,2002~2004年と2008~2010年を比較すると,第二世代抗精神病薬の使用が,4.9%から11.2%に増加し,第一世代抗精神病薬の使用は,17.4%から12.1%に減少していた.また,全体の抗精神病薬使用の普及率で調整後,抗精神病薬の使用は1.1倍増加していた,と報告した15).つまり,定型抗精神病薬の使用は減少したものの,非定型抗精神病薬の使用は増加しており,全体としての使用量は微増といった結果であった.
また,Arai, H.らは日本人AD患者に対する抗精神病薬の死亡リスクについて10,079例を対象とした前向き調査を行った1).357の医療機関で行われ,女性69%,平均年齢81歳が対象であった.登録の時点で抗精神病薬の使用歴が6ヵ月以上の割合が使用群の63.7%を占め,使用薬剤は非定型抗精神病薬ではクエチアピン,リスペリドン,オランザピンが多かった.特筆すべき点としては,新規投薬開始群では,服用開始11~24週で死亡率は9.4%,年齢・性別・体重などの要因を補正しても非服用群の2.5倍との結果であった.
これらの結果を受けて,本邦でもBPSDに対する抗精神病薬の使用について,厚生労働省が『かかりつけ医のためのBPSDに対応する向精神薬使用ガイドライン』として2013年に第1版を,2016年に第2版を発表した6).ここにおいては,非薬物的な介入を最優先にし,身体状況などを確認し,症候に応じて薬物を選択することが重要視されている.
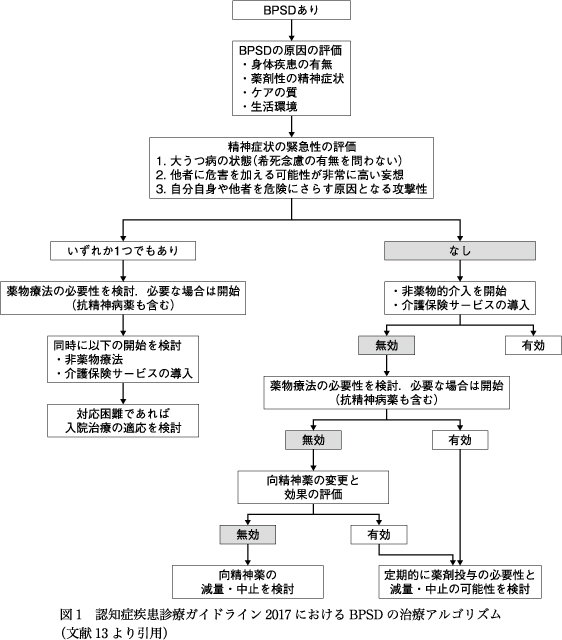
また,『認知症疾患診療ガイドライン2017』においても,BPSDがあった場合には,まず原因を評価し,緊急性がない場合は非薬物的な介入を優先させる,緊急性があった場合でも薬物療法と同時に非薬物療法の開始を検討する,とされている13)(図1).
III.非薬物療法の憂鬱
これまで述べてきたようにBPSDに対しては「抗精神病薬を使用する前に非薬物療法を検討する」というのが現在の大きなコンセンサスとなりつつある.一方で実臨床の場において,目の前に緊急性を要する易怒性や焦燥などのBPSDを有する患者がいるときにどのように非薬物療法を行えばいいのか,という問いへの答えは難しい.そもそも,非薬物療法は系統的な介入が難しくエビデンスが集約しづらく,実際にどのように行うべきかという指針が少ない.認知症の焦燥性興奮に対する33の非薬物療法の有効性を検証したシステマティックレビューでは,介護者がパーソンセンタードケアを学習したり,患者と適切に会話するスキルを学習したりすることが有用とされているが7),いずれも臨床医が緊急性を要する場面で現実的に活用できる非薬物療法ではない.その他としてグループ活動,音楽療法プログラム,タクティールⓇケア,マッサージなども挙げられているが,これらも同様であり,現実的に医師が実臨床の場ですぐに活用できるわけではない.臨床医はこのような二律背反の状況におかれているといえる.
IV.診断の再検討の重要性
ここで立ち返る必要があるのは,そもそもBPSDと一言で言ってもさまざまな病態が含まれており,単一の病態ではないという点である.BPSDという用語は認知症に健忘や認知機能障害以外の症状があることを説明する意味では有用であり,過去の「問題行動」といった誤解のある表現に代わる形で1996年に国際老年精神医学会によって提唱され3),その後普及した用語だが,逆にBPSDと呼ぶことで多彩な症状を十把一絡げにしてしまうおそれもある.
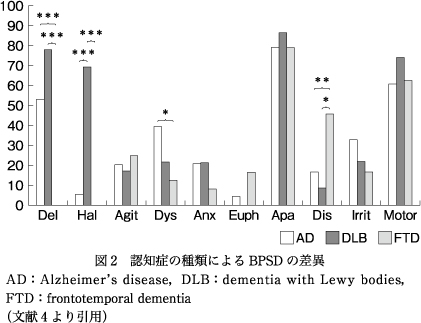
BPSDの種類は診断によっても大きく異なる.本邦のHirono, N.らはAD,レビー小体型認知症(dementia with Lewy bodies:DLB),前頭側頭型認知症(frontotemporal dementia:FTD)のBPSDをNeuropsychiatric Inventoryを用いて比較しており,例えばDLBでは幻覚妄想が目立つがFTDではほとんど目立たないなど,疾患の種類によってBPSDの様式が大きく異なることがわかる4)(図2).
診断が異なるということは,背景となる神経基盤も異なり,治療法が異なるということである.例えばDLBの幻視に対して抗精神病薬は副作用のリスクが大きく使うべきではない.一方でDLBの幻視に対してはコリンエステラーゼ阻害薬が有効との報告もあり10),診断によって治療方針が大きく異なる.一方でFTDの常同行動などの行動症状に対してはSSRIが有効という報告もエビデンスレベルは高くないが散見され2),これも検討の余地がある.
V.BPSDの出現に影響を与える因子
また,心理社会的な背景の理解や環境因の調整が重要なことはすでに多く述べられており言を俟たないが,それ以外のさまざまな要素もBPSDの出現に大きな影響を与える.例えば原因疾患をADに絞ったとしても,生物学的要因(遺伝的背景),中間要因(認知機能,年齢,ADL,身体状況,認知機能,内服薬),心理社会的要因(元来の性格,居住状況,婚姻状況,介護者負担感など)など多岐にわたった要素が影響する(図3).逆説的ではあるが,定型的な薬物療法に行き詰まったときこそ,症候の再検討,薬剤や身体状況などさまざまな因子の検討,診断の再考が重要と考えられる.
VI.新たな試み
そのような状況のなかで,著者らはBPSDの治療についていくつかの新しい試みを行っている.まずは前述のCATIE―ADの大規模データを用いたBPSDの薬物療法への反応予測因子の抽出の試みを行っている.例えばAD患者の精神病性症状や易怒性に対して抗精神病薬を投与した際の8週間後の治療反応は糖尿病,認知機能,身体機能,初期の精神症状の重症度が予測することを報告した11).また同様に認知機能が保たれていることが,AD患者の36週後の精神病性症状や易怒性などの症状の改善に寄与することも報告した12).このような情報は,実際に薬物療法を行ううえで大きな助けとなる.
また,「実際に役に立つ」非薬物的な介入をさがす試みも行っている.例えば書籍などでは「介助に抵抗する場合は今からすることを言葉に出して伝えましょう」とか「立ち上がってしまう場合には制止せずに声かけで誘導しましょう」などと対応法が提案されている.しかしながらそれらの有効性は確認されておらず,実際に有効なのか,あるいはどの程度の奏効確率で有効なのかは明らかにはされていない.一方,多彩なBPSDに対する色々な対応法の有効性を1つずつ,ランダム化比較試験で検証することは非現実的である.そこで,著者らは実臨床場面での有効性を明らかにすることをめざし,「認知症ちえのわnet」というウェブサイトを用い,そのために,「集合知」を活用するシステムを構築している14).これらの取り組みは将来のBPSDの予防・治療において重要であると考える.
おわりに
認知症のBPSDに対して薬物療法の前に非薬物的な介入を,という近年の流れの一方で緊急性のある状況で臨床医が用いることのできる非薬物療法が十分に提示されているわけではない.本邦では認知症患者への抗精神病薬投与に関して保険適用上の問題はあるが強い規制はない.そのため,BPSDに対する薬物療法としての抗精神病薬治療が依然として行われている経緯がある.だからこそ,薬物療法に行き詰まったときが,診断をあらためて再考し,BPSDに影響を与える身体状況や心理社会的要因などを再度検討するよい機会になると考える.
なお,本論文に関連して開示すべき利益相反はない.
1) Arai, H., Nakamura, Y., Taguchi, M., et al.: Mortality risk in current and new antipsychotic Alzheimer's disease users: large scale Japanese study. Alzheimers Dement, 12 (7); 823-830, 2016![]()
2) Buoli, M., Serati, M., Caldiroli, A., et al.: Pharmacological management of psychiatric symptoms in frontotemporal dementia: a systematic review. J Geriatr Psychiatry Neurol, 30 (3); 162-169, 2017![]()
3) Finkel, S. I., Costa e Silva, J., Cohen, G., et al.: Behavioral and psychological signs and symptoms of dementia: a consensus statement on current knowledge and implications for research and treatment. Int Psychogeriatr, 8 (Suppl 3); 497-500, 1996![]()
4) Hirono, N., Mori, E., Tanimukai, S., et al.: Distinctive neurobehavioral features among neurodegenerative dementias. J Neuropsychiatry Clin Neurosci, 11 (4); 498-503, 1999![]()
5) 本間 昭: 認知症の精神症状・行動障害 (BPSD) に対する抗精神病薬の使用実態に関するアンケート調査. 老年精神医学雑誌, 17 (7); 779-783, 2006
6) 厚生労働省: 「かかりつけ医のためのBPSDに対応する向精神薬使用ガイドライン (第2版)」について. 2015 (https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000135953.html) (参照2020-03-11)
7) Livingston, G., Kelly, L., Lewis-Holmes, E., et al.: Non-pharmacological interventions for agitation in dementia: systematic review of randomised controlled trials. Br J Psychiatry, 205 (6); 436-442, 2014![]()
8) Lopez, O. L., Becker, J. T., Chang, Y. F., et al.: The long-term effects of conventional and atypical antipsychotics in patients with probable Alzheimer's disease. Am J Psychiatry, 170 (9); 1051-1058, 2013![]()
9) Ma, H., Huang, Y., Cong, Z., et al.: The efficacy and safety of atypical antipsychotics for the treatment of dementia: a meta-analysis of randomized placebo-controlled trials. J Alzheimers Dis, 42 (3); 915-937, 2014![]()
10) Mori, E., Ikeda, M., Kosaka, K., et al.: Donepezil for dementia with Lewy bodies: a randomized, placebo-controlled trial. Ann Neurol, 72 (1); 41-52, 2012![]()
11) Nagata, T., Nakajima, S., Shinagawa, S., et al.: Baseline predictors of antipsychotic treatment continuation and response at week 8 in patients with Alzheimer's disease with psychosis or aggressive symptoms:an analysis of the CATIE-AD Study. J Alzheimers Dis, 60 (1); 263-272, 2017![]()
12) Nagata, T., Shinagawa, S., Nakajima, S., et al.: Association between neuropsychiatric improvement and neurocognitive change in Alzheimer's disease:analysis of the CATIE-AD Study. J Alzheimers Dis, 66 (1); 139-148, 2018![]()
13) 日本神経学会監: 「認知症疾患診療ガイドライン」作成委員会編: 認知症疾患診療ガイドライン2017. 医学書院, 東京, 2017
14) 認知症ちえのわnet. (https://chienowa-net.com/) (参照2019-09-02)
15) Okumura, Y., Togo, T., Fujita, J.: Trends in use of psychotropic medications among patients treated with cholinesterase inhibitors in Japan from 2002 to 2010. Int Psychogeriatr, 27 (3); 407-415, 2015![]()
16) Reus, V. I., Fochtmann, L. J., Eyler, A. E., et al.: The American Psychiatric Association Practice Guideline on the use of antipsychotics to treat agitation or psychosis in patients with dementia. Am J Psychiatry, 173 (5); 543-546, 2016![]()
17) Schneider, L. S., Dagerman, K. S., Insel, P.: Risk of death with atypical antipsychotic drug treatment for dementia: meta-analysis of randomized placebo-controlled trials. JAMA, 294 (15); 1934-1943, 2005![]()
18) Schneider, L. S., Tariot, P. N., Dagerman, K. S., et al.: Effectiveness of atypical antipsychotic drugs in patients with Alzheimer's disease. N Engl J Med, 355 (15); 1525-1538, 2006![]()
19) Wang, P. S., Schneeweiss, S., Avorn, J., et al.: Risk of death in elderly users of conventional vs. atypical antipsychotic medications. N Engl J Med, 353 (22); 2335-2341, 2005![]()