【目的】全国の保険請求の95%以上を網羅する「レセプト情報・特定健診等情報データベース(NDB)」のオープンデータを用い,クロザピン(CLZ)の使用実態を明らかにする.【方法】2014年度から2018年度のCLZの入院処方数と治療抵抗性統合失調症治療指導管理料の算定回数(外来+入院)を分析した.また管理料算定回数から患者数を推定し,さらに入院患者の平均投与量を調べた.【結果】CLZ 100 mg錠の総入院処方数は2015年度の82万錠から2018年度は171万錠に増えていた.25 mg錠を含めて100 mg錠に換算すると2018年度は196万錠で,人口千人あたり15.5錠であった.管理料の算定回数は2014年度が16,000回(外来50.3%),2018年度が39,000回(外来55.3%)に増え,CLZ使用患者数は1,330人から3,254人に増えた.2018年度の人口千人あたりの100 mg換算入院処方数は最多が沖縄62.9錠,最少が島根3.5錠であった.2018年度の人口千人あたり管理料の算定回数は全国で0.31回,最多は宮崎1.6回,最少は埼玉0.077回,人口10万人あたりのCLZ使用患者数は,最多の宮崎13.4人,最少の埼玉0.64人であった.2019年のクロザリル患者モニタリングサービス患者登録済み医療機関あたりの2018年度の管理料の算定回数は84.3回(1施設7.0人)で,最多は岡山で170回,最少は島根9回であった.2018年度の人口10万人あたりのCLZ使用患者数は男性2.8人,女性2.4人であり,男女とも35~39歳が多く,男性7.2人,女性6.6人であった.CLZ使用入院患者の1日あたり平均投与量は男性387 mg,女性348 mgであった.【考察】NDBオープンデータの性質上の限界はあるものの,CLZの使用患者数や都道府県別,性・年齢階級別の実態を明らかにできた.歴史的・制度的背景から海外と比べると使用患者数は少ないものの増加傾向であり,また地域差も縮小傾向ではあった.
2)国立研究開発法人国立国際医療研究センター国府台病院総合内科
3)国立研究開発法人国立国際医療研究センター国府台病院精神科
4)千葉大学医学部付属病院次世代医療構想センター
受理日:2021年9月20日
はじめに
クロザピン(clozapine:CLZ)は,治療抵抗性統合失調症に唯一適応をもつ抗精神病薬である.治療抵抗性とは,2種類以上の抗精神病薬を十分量・十分期間投与しても十分な反応が得られない,もしくは副作用によって抗精神病薬を十分な量まで増やせないものと定義される23).
CLZは抗精神病薬にしばしばみられる副作用である錐体外路症状の少ない非定型抗精神病薬として,1969年に世界各国での承認が開始されたが,重大な副作用の無顆粒球症のため1975年に発売ないし開発治験は中止された.しかし,治療抵抗性統合失調症の相当数がCLZには反応することが証明され,治療抵抗性症例に適応を限定して2009年に日本でも上市されることとなった24).CLZには無顆粒球症,心筋炎,心筋症,高血糖などさまざまな重大な副作用があり,無顆粒球症および耐糖能異常の早期発見,ならびに発現時の治療を目的として,発売と同時にクロザリル患者モニタリングサービス(Clozaril Patient Monitoring Service:CPMS)が導入された.これはCLZを使用する医療従事者,医療機関,保険薬局および患者を登録し,患者ごとの白血球数・好中球数および血糖値などのモニタリングの確実な実施を支援している29).
無顆粒球症などの血液障害は投与初期に発現する例が多く,原則投与開始18週間は入院管理下での投与が推奨されている25).CPMSの運用手順2)によると,血液検査の頻度は投与開始から26週までは週1回,その後は一定の条件を満たした場合でも2週に1回の実施が義務づけられており,無顆粒球症を呈した場合や発熱がみられる場合は,直ちに血液内科医に相談し,マニュアルに従った対応が必要となる.また,患者は血糖検査に基づき3区分され,「糖尿病もしくは糖尿病を強く疑う」基準の場合,血糖値は2週間ごと,HbA1cは4週間ごとに測定し,CLZ投与の妥当性を糖尿病内科医と検討する必要がある.頻回な血液検査や内科医との連携など,他の抗精神病薬と比較すると運用がはるかに複雑になっている.
厚生労働省の2017年患者調査によると,日本の医療機関で治療を受けている統合失調症患者数は79万人13)で,その20~30%が治療抵抗性と推定される17)ことから,治療抵抗性統合失調症は約16~24万人程度と予測され,CLZ治療に同意できる患者数はそのうちの3万人という推計もある4).CPMS登録患者数2)は2009年から2020年5月までののべ人数で10,266人であり,また精神保健福祉資料14)32)によれば2017年度にCLZを使用した患者数は,外来と入院を合わせて3,921人である.
日本ではCLZによる治療可能性がある患者に対して十分な治療がなされていない可能性があり,また諸外国と比較しても処方患者数がかなり少ない.また,都道府県別のCPMS登録患者数2)30)からみても大きな地域差が存在することが予想される.本研究の目的は,厚生労働省にて公開されている「レセプト情報・特定健診等情報データベース(NDB)」のオープンデータ12)を主に用いて,都道府県別,性・年齢階級別にCLZの使用実態を明らかにすることである.
I.研究の方法
1.NDB Open Data Japan(NDBオープンデータ)
レセプト情報・特定健診等情報データベース(National Database of Health Insurance Claims and Specific Health Checkups of Japan:NDB)に集積されている情報は,健康増進や医療費の適正化のために有益な情報を含んでおり,患者単位での詳細な解析もできるため,さまざまな研究に利用されている5)26).一方でNDBを利用するためには研究環境やデータハンドリングのスキルも必要であり,より簡便に広い主体によって入手・分析可能なNDBオープンデータを厚生労働省が公開しており,本研究ではこちらを用いた12).2016年度公開の第1回NDBオープンデータ(2014年度分レセプト情報および2013年度分特定健診情報)から,本稿執筆時点では2020年度公開の第5回(2018年度分レセプト情報および2017年度分特定健診情報)まで利用可能である.「医科診療行為」「歯科診療行為」「歯科傷病」「処方薬」「特定健診(検査値)」「特定健診(標準的な質問票)」の6つに大きく分かれ,特に「医科診療行為」では,医科入院/入院外レセプトおよびDPCレセプトの情報をもとに,厚生労働省告示の点数表で区分された各診療行為の算定回数について,「都道府県別」および「性・年齢階級別」に集計されている.なお都道府県は患者住所ではなく医療機関および薬局の住所である.「処方薬」については,医科入院/入院外レセプト,DPCレセプト,調剤レセプトの情報をもとに「内服」「外用」「注射」の剤形別に,「都道府県別」および「性・年齢階級別」に集計されている.薬価収載の基準単位に基づき,薬効分類別に処方数量の多い薬剤が公表され,第1回が全国での年間処方数上位30品目,第2回からは上位100品目となっている.都道府県別,性・年齢階級別の処方数については,ある項目が1,000未満の場合は公表されず,例えばある県でのCLZ 100 mg錠の入院処方が年間1,000錠未満であれば,その県の処方錠数は公開されない.同様に,加算などの算定回数は単体項目で10未満の場合は公開されない.ある薬剤や算定について,回数が少ないために非公開となる都道府県または年齢階級が1つだけの場合,全体の処方・算定回数と他の項目の合計から非公開の項目が計算できてしまうため,第1~4回は全体が非公開となり,第5回では最も少ない2ヵ所が非公開となっている.これまでにNDBオープンデータに基づく研究が精神神経分野を含めて,いくつも発表されている15)27)33).
2.解析方法
本研究では,NDBオープンデータから得たクロザリルⓇ 100 mg錠,25 mg錠の入院処方錠数を合算したCLZ 100 mg換算処方錠数と,治療抵抗性統合失調症治療指導管理料(以下,管理料)の算定回数をCLZ処方実態の指標として用いた.
CLZの添付文書25)には,初日は1日12.5 mgで1日200 mgまで漸増し,維持量は1日200~400 mg,最高用量は1日600 mgと記載されている.CLZは100 mg錠と25 mg錠の規格があるが,25 mg錠は処方数が少なく,データの公開は2017年度,2018年度の入院のみであった.また,CLZ 100 mg処方錠数はデータが2015年度から2018年度の入院に限られ,外来データは公開されていない.さらに都道府県別については,データが2016年度,2018年度のみに限られている.
管理料は,CLZを投与している治療抵抗性統合失調症患者に対して,月1回に限り算定できる.管理料については,2014年度から2018年度の5年間のデータが入院・外来別に公開されており,入院と外来を合わせた算定回数を分析に用いた.ただし,2015年度は算定回数が10未満の都道府県が1つあったため,都道府県別の入院のデータは公表されていない.CLZ使用患者には2週に1回の血液検査が義務づけられており2),管理料は入院・外来問わず月1回算定できるので,すべての患者が1年間に12回算定されたと仮定し,各年度の算定回数からCLZを使用した患者数(以下,CLZ使用患者数)を入院・外来別に推計した.さらに,CLZ 100 mg換算処方錠数をCLZ使用患者数(入院)で割り,CLZ使用患者(入院)1人あたりの処方錠数/日や投与量/日を求めた.
都道府県別の分析については,2016年度,2018年度のCLZ 100 mg換算処方錠数,2014年度,2016年度,2017年度,2018年度の管理料算定回数を,それぞれ人口千人あたりで算出した.管理料については,CPMSの地方区分を踏まえて,全国を北海道・東北,関東,中部,関西,中国・四国,九州・沖縄の6地方に分け,地方ごとに人口千人あたりの算定回数を算出した.ただし,2014年度の三重,島根,山口のデータは算定回数が10回未満であり,公表されていない.さらに人口10万人あたりのCLZ使用患者数を都道府県別に算出した.また,2019年8月のCPMS患者登録済み医療機関数2)を分母にとり,2018年度の各都道府県の登録機関あたりの管理料算定回数を算出した.
性・年齢階級別の分析に関しては,2015年度から2018年度のCLZ 100 mg換算処方錠数,2014年度から2018年度の管理料の算定回数を,5歳階級ごとに男女計・男性・女性について,人口千人あたり,およびCLZ使用患者(入院)1人あたりで算出した.
上記の各指標の算出において,総務省統計局が公表している各年10月1日の人口推計を用いた.
本研究は国立国際医療研究センター倫理審査委員会の承認を得て行った(承認番号:NCGM-G-003402).
II.結果
CLZ 100 mg入院処方錠数について,各年度の比較のため25 mg錠を除くと,2015年度は82万錠,2016年度は93万錠,2017年は111万錠,2018年度は171万錠であり,3年間で約2倍に増加した.25 mg錠を含めて100 mg錠に換算すると2018年度は196万錠であった.管理料の算定回数(入院+外来)は2014年が16,000回,2018年が39,000回と2倍以上になっており,CLZ 100 mg処方錠数と同様に増加傾向であった.また,外来の割合は50.3%から55.3%に増加していた.管理料の算定回数から推計したCLZ使用患者数は2014年度が1,330人,2018年度が3,254人であった.CLZ使用患者(入院)1人あたりの処方錠数/日は各年度の比較のため25 mg錠を除くと2015年度から2018年度でそれぞれ2.7錠,2.6錠,2.6錠,3.2錠であった.25 mg錠を含めて100 mgに換算すると2018年度は3.7錠であった.
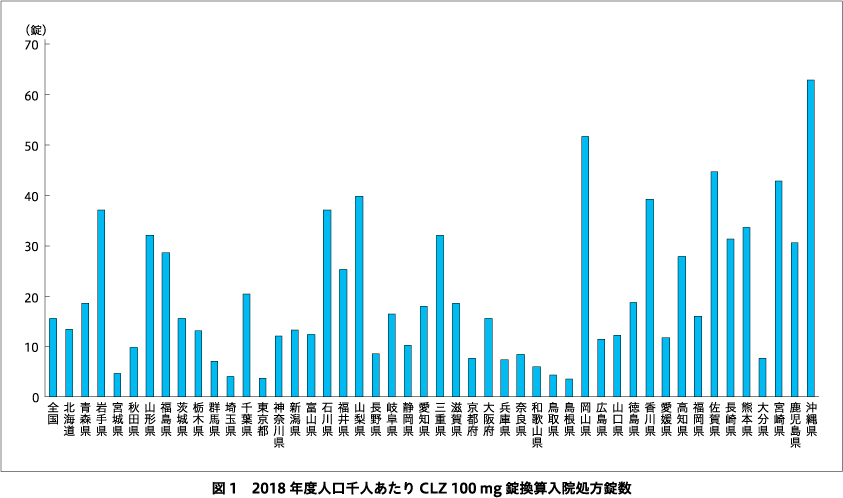
2018年度のCLZ 100 mg換算処方錠数は人口千人あたり15.5錠であった.都道府県別にみると(図1),最多は沖縄で62.9錠(全国平均の4.1倍),岡山51.7錠(3.3倍),佐賀44.7錠(2.9倍)と続き,最少は島根で3.5錠(全国平均の0.23倍),東京3.7錠(0.24倍),埼玉4.0錠(0.26倍)であった.2016年度のCLZ 100 mg処方錠数は最多の沖縄が全国平均の6.0倍で,島根と徳島は処方錠数が年間1,000錠未満で公開されなかった点からは,地域差は縮小傾向といえる.
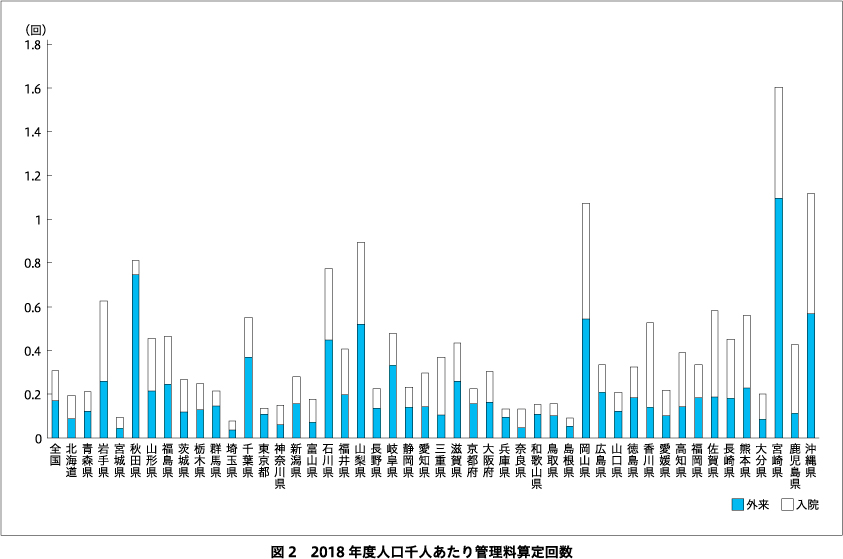
また,2018年度の管理料の算定回数(外来+入院)は,外来は22,000回,入院は17,000回で,人口千人あたり合計0.31回であった.都道府県別の管理料の人口千人あたり算定回数(図2)は,最多は宮崎1.6回(全国平均の5.2倍),沖縄1.1回(3.5倍),岡山1.1回(3.5倍)と続き,最少は埼玉0.077回(0.25倍),島根の0.093回(0.30倍),宮城0.094回(0.31倍)と続いた.2014年度は最多の宮崎が全国平均の6.6倍で,最少の神奈川は0.06倍であり,人口あたりの管理料算定回数からみても地域差は縮小傾向といえる.
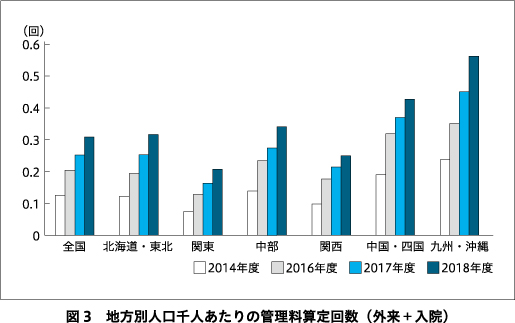
2018年度の管理料から算出した人口10万人あたりのCLZ使用患者数は,最多は宮崎13.4人,沖縄9.3人,岡山8.9人,最少は埼玉0.64人,島根0.77人,宮城0.79人であった.外来と入院の割合にも地域差があり,外来の割合が最大は秋田92%,東京79%,兵庫72%,最小は鹿児島26%,香川27%,三重29%であった.次に,地方ごとの人口千人あたりの管理料算定回数を図3に示したが,最多は九州・沖縄で0.56回(人口10万人あたりのCLZ使用患者数4.7人),最少は関東で0.21回(人口10万人あたりのCLZ使用患者数1.7人)と約3倍の格差がみられた.2014年度から2018年度までの年次推移をみるとすべての地方で増加しているが,最少の関東は2.6倍,最多の九州・沖縄は2.3倍に増えており,地域差は縮小傾向ともいえる.ただし,全国平均を基準に比較すると,最少の関東は全国平均の0.67倍から0.60倍に,最多の九州・沖縄は,1.8倍から1.9倍と地域差が拡大傾向ともいえ,一貫した結果ではなかった.
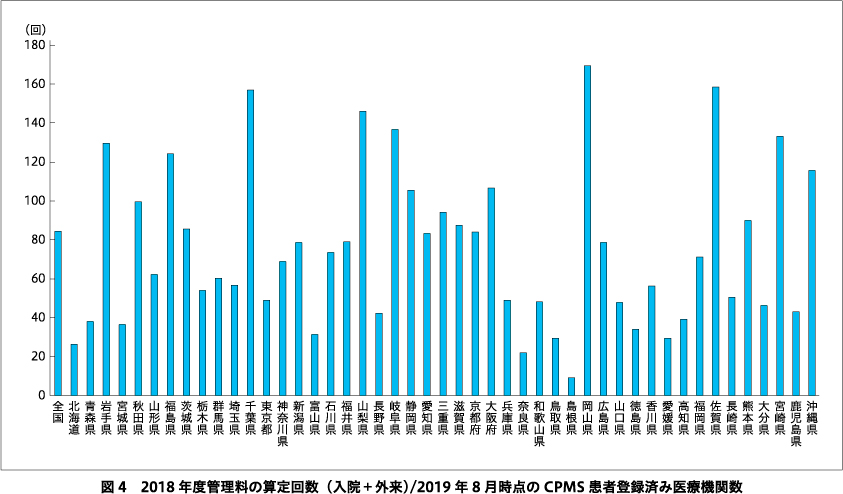
都道府県別のCPMS患者登録済み医療機関(2019年8月)あたりの2018年度の管理料の算定回数は84.3回(患者数としては1施設7.0人)で,都道府県別にみると最多は岡山で170回(全国平均の2.0倍),佐賀159回(1.9倍),千葉157回(1.9倍)と続き,最少は島根9回(0.11倍),奈良22回(0.26倍),北海道26回(0.31倍)と続いた(図4).
男女別にみると,2015年度から2018年度にかけてのCLZ 100 mg処方錠数は,各年度の比較のため25 mg錠を除くと,人口千人あたり男性がそれぞれ7.9錠,9.1錠,10.8錠,16.7錠,女性がそれぞれ5.0錠,5.5錠,6.7錠,10.6錠と男女ともに増加傾向で男性のほうが多かった.25 mg錠を含めて100 mg錠に換算すると2018年度は男性18.9錠,女性12.3錠であった.2014年度から2018年度にかけての管理料の算定回数(入院+外来)については,人口千人あたり男性がそれぞれ0.14回,0.18回,0.22回,0.27回,0.33回,女性がそれぞれ0.12回,0.15回,0.19回,0.24回,0.29回と経年的に増加傾向であった.2018年度の人口10万人あたりのCLZ使用患者数は男性2.8人,女性2.4人であり,CLZ使用入院患者1人あたりの投与量(/日)は男性387 mg,女性348 mgであった.
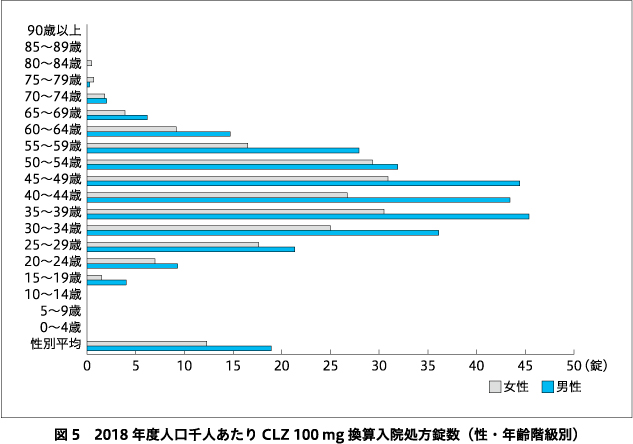
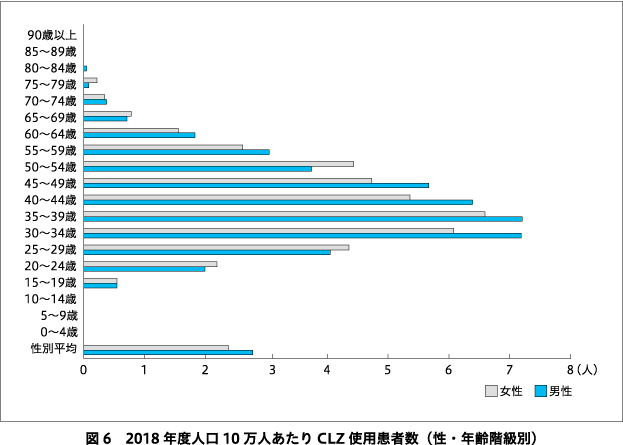
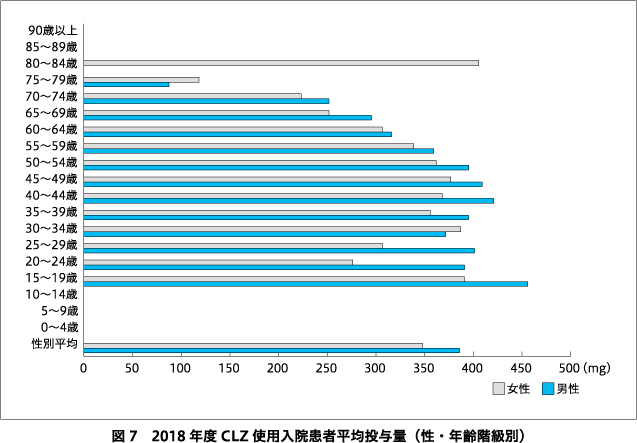
年齢階級別にみると,2018年度,人口千人あたりのCLZ 100 mg換算処方錠数が多かった年代は(図5),男女ともに30~50代であり,男性で最も多かった35~39歳では45.4錠,女性で最も多かった45~49歳では30.9錠だった.男女問わず0~14歳,男性では80歳以上,女性では85歳以上では処方が1,000錠未満で少ないためデータが公開されていない.人口10万人あたりのCLZ使用患者数(入院+外来)が多かった上位3つの年齢階級は(図6),男女ともに30~34歳,35~39歳,40~44歳であり,年齢階級順に男性が7.2人,7.2人,6.4人,女性が6.1人,6.6人,5.4人であった.男女ともに0~14歳,85歳以上では,算定回数は10回未満であるため公開されていない.CLZ使用入院患者1人あたりの投与量(/日)(図7)は,男女ともに15~19歳で男性457 mg,女性392 mgと多く,またほとんどの年代で男性の投与量が女性より多く,高齢になると投与量は少なくなっていた.ただし女性の80~84歳は入院患者数が少ないため,投与量が極端に多い結果となった.
III.考察
本研究において,CLZの処方数,管理料の算定回数はともに増加傾向であり,2018年度の推定使用患者数は3,254人とCLZの使用は経年的に拡大していた.2014年度から2018年度までに算定回数の外来の割合は50.3%から55.3%に増加していた.経年的には地域差は縮小傾向ではあるものの,都道府県間では大きなばらつきがみられ,人口千人あたりの算定回数(入院+外来)でみると特に九州・沖縄地方でCLZが普及していた.また,性別でみると男性のほうがCLZ使用患者数も入院患者1人あたりの投与量も多かった.年齢階級別については,CLZ 100 mg換算処方錠数,算定回数は男女ともに30~50代にピークがみられ,入院患者では高齢になるほど投与量が減少傾向であった.
1.CLZの普及について
CLZの普及率の低さは多くの国で指摘されており,さらに各国の差も顕著である.日本を含む17ヵ国における2014年の人口10万人あたりのCLZ使用頻度の比較1)では,最も高い国はフィンランド189人,ニュージーランド116人と続き,アジアでは台湾で88人であったが,日本は最下位で0.6人であった.この研究では外来患者のみを対象としているため,入院患者の多い日本での使用頻度が過小評価されている面もあるが,われわれのデータでも2018年度の推定使用患者は人口10万人あたり2.6人であり,諸外国と比較すると,日本はいまだに大きな遅れをとっているのが現状である.その理由としては,CLZ導入が遅れたことや厳しい規制などが考えられている.日本では1995年に治験が開始され,2004年に承認申請がされたものの,使用ガイドラインの作成やそれに従った治験の実施にあたって規制当局と学会の論議があり,実際に上市されたのは2009年であった18).これは,米国と比較すると19年遅れている.またCLZ規制の各国の比較によると,白血球数・顆粒球数が安定しているCLZ維持療法中の患者における血液モニタリング頻度が海外で1ヵ月ごとであるのに対し,日本では2週間ごととなっており,日本では世界に類をみないほど厳しい規制がある.それに加え,ほとんどの国ではCLZを扱う製薬会社が複数あるのに対し,日本ではノバルティスファーマ1社であり,日本で普及が遅れている原因と考えられている22).
一方で,本研究ではCLZ 100 mg処方錠数は3年間で約2倍,管理料の算定回数は4年間で2倍以上に増加していた.CLZ使用患者数は2014年度から2018年度で1,330人から3,254人に増えており,CLZの普及は確実に進んでいる.CLZの普及により長期入院精神障害者の地域移行や,精神科病床の平均在院日数の短縮化が期待されているが4,21),管理料算定回数に占める外来の割合は,地域差は大きいものの全体としては50.3%から55.3%に増加し,推計外来患者も670人から1,801人に増加している.
CLZの普及促進のため,本邦ではさまざまな制度の改正が行われてきた.CPMSの運用ルールにおいては,2014年に登録通院医療機関の新設により入院設備がない医療機関などにおいてもCLZの処方が可能となる,2017年に中止基準による投与中止後の患者もクロザリル適正使用委員会に承認された場合に再投与が可能になる,2018年に血液内科医以外の内科医とも連携が可能になる,など頻繫に改定がなされてきた2).また,2018年度の診療報酬改定では,「精神療養病棟入院料」「地域移行機能強化病棟入院料」などのCLZの薬剤料を包括範囲から除外して出来高算定が可能になり,CLZ処方患者の増加の大きな要因と考えられる.
さらに2020年度には,同一保険医療機関内で転棟する場合もCLZの新規導入患者であれば精神科救急入院料などが算定できる,精神科救急入院料などにおける自宅などへの移行率からCLZの新規導入患者を除外するなどの診療報酬改定が行われた.これによりCLZの導入のための転棟がしやすくなり,入院期間が3ヵ月を超える場合や転院が必要な場合も,在宅移行率が下がることがなくなった.同時に,CLZを投与中の患者に対してはHbA1cを月1回に限り別に算定できるようになるなどの見直しが行われた.2021年6月にはCLZ添付文書が改定され,血液モニタリングについて条件つきで52週以降,4週間隔の検査が可能となる,投与基準について既往歴(無顆粒球症,重度好中球減少症)のある患者への投与が可能となるなどの緩和が行われ25),今後CLZのさらなる普及が期待できる.
2.CLZの投与量について
CLZの維持量は200~600 mgだが,本研究における2018年度のCLZ使用患者(入院)1人あたりのCLZ投与量(/日)は,370 mgであった.導入期の入院患者も含んでおり,外来で維持量を内服している患者の投与量はさらに多い可能性はある.2009年から2016年にCPMSに登録された3,746人を対象とした研究16)では,白血球・好中球減少をきたさなかった3,526人の最大投与量は平均387.5 mgであり,2009年から2015年の製造販売後調査28)の新規投与開始例1,860人の平均投与量は322 mgであり,われわれのデータと大きな差はないと考えられる.
3.地域差について
CPMS患者登録済み医療機関数や登録済み医療機関あたりの患者数において,地域差があることは以前から指摘されており,2018年度の各都道府県別のCPMS患者登録済み医療機関数を人口10万人あたりで比較し,最多が宮崎1.2施設,最少が埼玉の0.14施設であったことなどが報告されている2)30).本研究においてもCLZの使用には都道府県ごとに大きな格差がみられた.CLZ 100 mg処方錠数に関しては,最多の沖縄と最少の島根では約18倍の格差がある.一方,2015年度NDBオープンデータを用いて外来処方された抗精神病薬のクロルプロマジン換算値の地域差を調べた研究19)では,投与量が最多の長野は最少の奈良の1.9倍であり,CLZほど格差は顕著ではなかった.また,2018年度CPMS患者登録済み医療機関あたりの管理料算定回数は,最多の岡山は最小の島根で約19倍であり,大きな地域差がみられた.外来と入院の割合に注目すると,外来の割合が多い秋田や東京では,治療抵抗性統合失調症患者の地域移行の成功の可能性が示唆される.このように,CLZの処方数は他の抗精神病薬と比較して極端に大きな地域差がみられるが,有病率の地域差や医師のプラクティスが均てん化されていないことだけではなく,CPMSへの対応を含めた医療体制の地域差が大きく影響していると考えられる.NDBオープンデータでは都道府県単位の分析しかできないが,NDBを用いた地域精神保健医療福祉社会資源分析データベース(ReMHRAD)では二次医療圏ごとに分析されている32).CLZ処方の地域差については海外でも問題となっており,フランスの保険データベースを用いた研究では,CLZがほとんど処方されていない地域も,全国平均の6倍近く処方されている地域もあった31).
2018年度に全国のCPMS登録医療機関222施設に行われたアンケート調査9)では,施設ごとの累計患者数は9人以下が半数を超えており,CPMSに登録済みであってもCLZ治療がそれほど行われていない施設が多い.また,CLZ治療をするうえでの障壁に関して,30%以上の施設が該当していると回答した項目は,「血液検査の回数が多い」「CPMSの入力が煩雑である」「無顆粒球症などの副作用が心配である」「血液内科や糖尿病を治療する内科などの身体科との連携に不安がある」「患者もしくは代諾者の同意が得られない」などであった.CLZ導入時や投与中の管理が煩雑であることによる精神科医の処方態度の相違だけでなく,医療体制や医療連携の相違などが地域差に現れていることが考えられる.2017年厚生労働省の難治性精神疾患地域連携体制整備事業のモデル事業に,沖縄,岡山,兵庫,大阪,三重,千葉から6地域が選ばれている.これらの地域では,CLZの使用についても拠点病院や協力病院の役割があり,身体科も含めた病院間の良好なネットワークが整備されていた.また,木田らの政策研究ではCLZ症例数が多い好事例病院として,宮崎,愛知,山梨,秋田,沖縄の病院が取り上げられている9).これらの好事例病院では,院内においてCLZ委員会の設置,治療マニュアルの使用,クリニカルパスの使用,CLZ専門病棟などの体制が整備されていた.好事例地域や好事例病院がある地域は本研究で処方数や管理料の算定回数が多かった都道府県と一致しており,CLZが使用しやすい環境であるか否かで地域差が生まれていることがわかる.CLZ治療に積極的に取り組んでいる好事例病院7-9)20)の工夫やノウハウなどを,各都道府県・各施設で取り入れることなどが,地域差の是正につながると考える.
4.年齢分布について
CLZの添付文書25)には,高齢者には慎重投与,妊娠中の投与に関する安全性は確立していない,授乳を避けること,小児に対する有効性および安全性は確立していない,とある.
本研究では,未成年および高齢者ではCLZ使用患者は少なかった.高齢者は「抗コリン作用による尿閉・便秘等があらわれやすく,また特に循環器機能が低下している高齢者では起立性低血圧や頻脈があらわれやすい」と記載されている.そのため,身体機能の低下や身体疾患の合併率の増加に伴い,他の年代と比べてCLZの導入,継続が困難である症例が多いことや加齢に伴う統合失調症の症状の変化が考えられる.17ヵ国を比較した報告1)でも,CLZ使用患者は30~59歳にピークがある国が多く,日本のCPMS登録患者3,780人の平均は40.6歳であった6).
さらに,CLZの血中濃度は40歳を境に5歳年齢が上がるごとに4%増加,5歳年齢が下がるごとに5%減少するとの報告3)があり,高齢になるにつれて投与量が減少すると考えられる.本研究の結果と矛盾しない.
5.性差について
2018年度の人口10万人あたりのCLZ使用患者数は男性が女性の1.2倍と多く,CPMS登録患者3,780人のうち男性は53.7%であり6),日本では男性のほうがわずかに多いが,17ヵ国を比較したデータでは男性が1.5倍という結果であった1).
CLZ使用入院患者1人あたりの投与量(/日)は,男性は女性の1.1倍であった.CLZの血中濃度は,女性が男性に比べて17%増加すると報告3)があり,本研究と矛盾しない.また,喫煙はCLZの代謝酵素であるCYP1A2を誘導し,CLZの血中濃度を低下させたとの報告3)34)がある.国民健康・栄養調査11)によると,2019年度の成人喫煙率は男性が29.0%,女性が8.1%であり,男性は女性と比較し喫煙者が多いため,投与量が多いと考えられた.さらに,CLZの血中濃度は体重80 kgを境として体重が10 kg増えるごとに5%減少,10 kg減るごとに5%増加するとの報告が3)あり,一般的に男性は女性より体重が重いため投与量が多いと考えられた.
6.本研究の限界と強みについて
第一に,患者個人単位での解析が可能なNDBの特別抽出データと異なり5)26),NDBオープンデータではCLZの全国での年間処方錠数や,都道府県別,性・年齢階級別の年間処方錠数しか公開されていない.そのため,何人の患者に処方されたか,1人あたりの投与錠数がどの程度あったか,年度途中での処方の開始,中断,終了などは解析不能である.海外と比較して普及が遅れていることも踏まえて,必要な患者に処方されていないことを問題として研究を行ったが,治療効果や副作用などのアウトカムデータはなく,過剰または不適切な使用や,副作用のリスクについては検討できない.ただし,CLZ処方患者のみを対象とし,外来でも入院でも月1回算定できる管理料を利用することで,処方患者数の推定や,平均処方錠数の推定を行うことができた.推定患者数に関しては,12回の算定回数を1人としており,年度途中での開始や中断などを考えると,実際の患者数はより多いことが考えられる.
第二に,NDBでは,医療費が公費負担である生活保護受給者や医療観察法患者が除外されている.統合失調症患者は生活保護受給者の割合が高く,また,医療観察法患者の入院医療を担う指定入院医療機関30施設に行われたアンケート調査10)では,一般精神科病床よりCLZ使用患者が多い.NDBから集計表として作成された一方でNDBオープンデータは保険診療の大部分をカバーしており,悉皆調査に近いデータが得られるものの,上記の公費負担の患者が除外されており,結果を過小評価している可能性は否定できない.
第三に,処方錠数や算定回数が少ない場合はデータが公表されていない.CLZは100 mg錠と25 mg錠の規格があるが,25 mg錠は処方錠数が少なく,精神神経用剤の処方数上位100位以内ではないため,データが公開されていない年度がある.また100 mg錠も外来での処方は上位100位以内ではないためデータが公開されていない.入院処方の100 mg錠が主な解析対象であるが,導入期で少量から開始している患者と,すでに維持量を用いているが,副作用,精神的または身体的な問題で入院した患者を区別することはできない.入院患者の平均投与錠数については,導入のため投与量が少ない患者が含まれること,月の途中で入退院した患者も含まれること,25 mg錠が年度によってデータに含まれていないことなどから,過小評価になっている可能性がある.
最後に,CPMS患者登録済み医療機関数については月が替わるごとに最新のデータが公表されているが,過去のデータは公開されていない.そのため2018年度NDBオープンデータと2019年8月のCPMS患者登録済み医療機関数を組み合わせて解析しており,経年的に患者数が増えていることも含めて正確なデータとはいえない.この点,正確な現状を可視化する意味でもCPMS患者登録済み医療機関数について過去のデータが公開されることが望ましいと考える.
しかし,本研究の強みとして,NDBオープンデータは全国を網羅しており国民レベルの分析が経年変化も含めて実施できたこと,入院患者の平均投与量や都道府県別,性・年齢階級別の使用実態など過去に十分調べられていないデータが得られたこと,既存の大規模研究のデータとあまり乖離がなくある程度の精度があること,NDBオープンデータを用いたCLZの処方実態の研究はこれまでに発表されていないこと,などが挙げられる.
おわりに
日本におけるCLZの普及の遅れ,地域差については以前から議論されていたが,本研究でもそれを裏づける結果が出た.またCLZ使用入院患者の平均投与量が明らかになった.さらに性・年齢階級別にみると,CLZ使用患者数や,CLZ使用入院患者の平均投与量は男性のほうが多いこと,小児や高齢者への処方数は少なく,30~40代にピークがみられることがわかった.CLZの処方は,経年的に縮小傾向ではあるのものの都道府県ごとの格差が著明であるが,普及は確実に進んでおり,今後の均てん化が期待される.
本研究の要旨は第116回日本精神神経学会学術総会(仙台)において研修医および学部学生による演題として発表した.
なお,本論文に関連して開示すべき利益相反はない.
1) Bachmann, C. J., Aagaard, L., Bernardo, M., et al.: International trends in clozapine use: a study in 17 countries. Acta Psychiatr Scand, 136 (1); 37-51, 2017![]()
2) クロザリル適正使用委員会: (http://www.clozaril-tekisei.jp) (参照2021-10-11)
3) Couchman, L., Morgan, P. E., Spencer, E. P., et al.: Plasma clozapine, norclozapine, and the clozapine: norclozapine ratio in relation to prescribed dose and other factors: data form a therapeutic drug monitoring service, 1993-2007. Ther Drug Monit, 32 (4); 438-447, 2010![]()
4) 榎本哲郎, 伊藤寿彦, 早川達郎ほか: 治療抵抗性統合失調症に対する治療戦略―日本におけるクロザピン治療の現状と課題―. Prog Med, 33 (11); 2341-2345, 2013
5) Hirose, N., Ishimaru, M., Morita, K., et al.: A review of studies using the Japanese National Databese of Health Insurance Claims and Specific Health Checkups. Ann Clin Epidemiol, 2 (1); 13-26, 2020
6) Inada, K., Oshibuchi, H., Ishigooka, J., et al.: Analysis of clozapine use and safety by using comprehensive national data from the Japanese clozapine patient monitoring service. J Clin Psychopharmacol, 38 (4); 302-306, 2018![]()
7) 伊豫雅臣: Q84千葉クロザピン・サターンプロジェクト. クロザピン100のQ & A (藤井康男編). 星和書店, 東京, p.248-250, 2014
8) 木田直也, 村上 優, 大鶴卓ほか: 地域におけるclozapine治療ネットワーク―琉球病院を拠点とした沖縄モデル―. 臨床精神薬理, 21 (11); 1439-1449, 2018
9) 木田直也: 重度かつ慢性の精神障害者に対する包括的支援に関する政策研究―クロザピン使用指針研究―(総括報告書). 平成30年度厚生労働科学研究費補助金〔障害者政策総合研究事業(精神障害分野)〕重度かつ慢性の精神障害者に対する包括的支援に関する政策研究―クロザピン使用指針研究(H29―精神―一般―005)平成30年度総括・分担研究報告書(研究代表者: 木田直也). p.1-20, 2019
10) 来住由樹, 矢田勇慈, 北川航平ほか: 治療抵抗性統合失調症に対する効果的かつ安全な治療法の確立に関する研究. 平成29年度国立研究開発法人日本医療研究開発機構委託研究開発事業(精神障害分野)医療観察法における, 新たな治療介入法や, 行動制御に係る指標の開発等に関する研究(研究代表者: 平林直次)研究開発分担報告書. 2017
11) 厚生労働省: 国民健康・栄養調査. (https://www.mhlw.go.jp/bunya/kenkou/kenkou_eiyou_chousa.html) (参照2021-10-11)
12) 厚生労働省: NDBオープンデータ. (https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000177182.html) (参照2021-10-11)
13) 厚生労働省: 平成29年(2017)患者調査の概況. (https://www.mhlw.go.jp/toukei/saikin/hw/kanja/17/dl/01.pdf) (参照2021-10-11)
14) 厚生労働省社会・援護局障害保健福祉部精神・障害保健課, 国立精神・神経医療研究センター精神保健研究所: 精神保健福祉資料. (https://www.ncnp.go.jp/nimh/seisaku/data/) (参照2021-10-11)
15) Kumamaru, K. K., Machitori, A., Koba, R., et al.: Global and Japanese regional variations in radiologist potential workload for computed tomography and magnetic resonance imaging examinations. Jpn J Radiol, 36 (4); 273-281, 2018![]()
16) Matsui, K., Ishibashi, M., Kawano, M., et al.: Clozapine-induced agranulocytosis in Japan: changes in leukocyte/neutrophil counts before and after discontinuation of clozapine. Hum Psychopharmacol, 35 (4); e2739, 2020![]()
17) Meltzer, H. Y.: Clozapine: balancing safety with superior antipsychotic efficacy. Clin Schizophr Relat Psychoses, 6 (3); 134-144, 2012![]()
18) 三國雅彦: クロザピン療法―承認が遅れた要因の検討ならびにその作用機序の解明研究の展望―. 精神医学, 60 (12); 1327-1338, 2018
19) 南園佐知子, 野村恭子: 外来処方向精神薬の等価換算値の性・年齢・地域分布―第2回NDBオープンデータベースから―. 秋田県公衆衛生学雑誌, 15 (1); 13-21, 2019
20) 宮田量治, 三澤史斉, 藤井康男ほか: 長期在院者の退院促進実績を有する日本の「好事例病院」におけるclozapine使用状況. 臨床精神薬理, 23 (1); 15-24, 2020
21) 水野謙太郎, 末金 彰, 長友恭平ほか: 単科精神科病院における脱施設化とclozapineの役割. 臨床精神薬理, 23 (1); 53-61, 2020
22) Nielsen, J., Young, C., Ifteni, P., et al.: Worldwide differences in regulations of clozapine use. CNS Drugs, 30 (2); 149-161, 2016![]()
23) 日本神経精神薬理学会編: 統合失調症薬物治療ガイドライン 医学書院, 東京, 2016
24) ノバルティスファーマ株式会社メディカル情報・コミュニケーション部: Q34欧米や日本での導入の歴史を教えて下さい. クロザピン100のQ & A (藤井康男編). 星和書店, 東京, p.102-103, 2014
25) ノバルティスファーマ株式会社: クロザリル錠25 mg, 100 mg添付文書. 2021年6月改訂(第2版).
26) Okumura, Y., Sakata, N.: Antidementia drug use in Japan: bridging the research-to-practice gap. Int J Geriatr Psychiatry, 33 (9); 1286-1287, 2018![]()
27) 佐藤愛子, 吉村健佑: NDBオープンデータを用いた向精神薬の処方分析. 臨床精神薬理, 24 (1); 27-41, 2021
28) 鳥山和宏, 三上智己, 佐藤欣久ほか: 治療抵抗性統合失調症患者を対象としたclozapineの製造販売後調査結果(最終報告). 臨床精神薬理, 22 (11); 1107-1139, 2019
29) 鳥山和宏, 秋葉達彦, 金井悠夏ほか: Clozapine治療におけるCPMSの役割. 臨床精神薬理, 23 (1); 71-83, 2020
30) 辻野尚久: Clozapine治療の地域偏在と均てん化に向けて. 臨床精神薬理, 23 (1); 63-70, 2020
31) Verdoux, H., Pambrun, E., Cortaredona, S., et al.: Geographical disparities in prescription practices of lithium and clozapine: a community-based study. Acta Psychiatr Scand, 133 (6); 470-480, 2016![]()
32) 山之内芳雄: Clozapine導入促進と日本の精神保健福祉政策. 臨床精神薬理, 23 (1); 3-14, 2020
33) Yoshimura, K., Hashimoto, T., Sato, Y., et al.: Survey of anticonvulsant drugs and lithium prescription in women of childbearing age in Japan using a public national insurance claims database. Clin Neuropsychopharmacol Ther, 9; 20-28, 2018
34) Zullino, D. F., Delessert, D., Eap, C. B., et al.: Tobacco and cannabis smoking cessation can lead to intoxication with clozapine or olanzapine. Int Clin Psychopharmacol, 17 (3); 141-143, 2002![]()