超高齢社会を迎えたわが国では,高齢者の増加にあわせて,認知症の人への支援体制の整備が緊急の課題である.そのなかで,従来悪性腫瘍への対応を中心に展開してきた緩和ケアを認知症ケアに応用する試みが進められている.緩和ケアは,苦痛の予防と苦痛からの解放を目的とした医療・ケアである.特に重視をするのは,疾病の経過(illness trajectory)を把握し,今後の経過を予測したうえで,起こりうる課題を予測・対処するとともに,本人の意向を尊重することで,療養生活の質(QOL)を最大化させることをめざす.特に,認知症に応用するに際しては,コミュニケーションの障害から起こりうる身体的苦痛への対応と,本人が自己決定できる早期の段階において,今後起こりうることを話し合い,療養生活の方針に反映させるアドバンス・ケア・プランニングが強調される.今後,急性期医療や在宅医療の現場において,広く認識・実践されることが望まれる.
はじめに
認知症は,単に認知機能の問題にとどまらず,生命予後を規定する病態でもある.経過を追うと,身体・精神機能の低下は不可逆的であり,最終的に死は避けられない.このような予後が規定された段階〔エンドオブライフ(End of Life)〕では,積極的な治療は療養中の生活の質(quality of life:QOL)の向上に寄与しないばかりか,苦痛を増すだけになる.
この時期に適応できるのは緩和ケアのアプローチである.緩和ケアは,身体的,精神的,社会的,実存的な苦痛を包括的にアセスメントし,マネージすることで,患者のみならず,その家族の療養中のQOLの向上をめざす試みである.緩和ケアには,当事者・家族と疾病や予後に関する話し合い,アドバンス・ケア・プランニング(advance care planning:ACP)も含まれる50).ヨーロッパ緩和ケア学会(European Association for Palliative Care:EAPC)は,2013年に認知症の緩和ケアに関する提言を公開し,11の領域で57の提言を掲げ,ヨーロッパ各国で認知症の緩和ケアが向かうべき方向を強調している50).諸国の状況を知ることは,わが国が認知症にどのように取り組むかを考えるうえで,示唆に富むものである40).
本稿では,特に終末期を含めたエンドオブライフ(一般的に身体精神機能の低下がもはや避けることが難しい段階を指す)の検討をまとめたい.
I.緩和ケアとは
世界保健機関(World Health Organization:WHO)が2002年に緩和ケアの定義を「緩和ケアとは,生命を脅かす病に関連する問題に直面している患者とその家族のQOLを,痛みやその他の身体的・心理社会的・スピリチュアルな問題を早期に見出し的確に評価を行い対応することで,苦痛を予防し和らげることを通して向上させるアプローチである」(緩和ケア関連団体会議定訳)と定めている57).
この定義で注目する点は,
①緩和ケアの目標が,「苦痛の予防と苦痛からの解放」にあること
②緩和ケア的アプローチは,病気の早い時期にも適応できること
の2点である.従来の緩和ケアは,終末期において痛みを緩和することが主眼であったが,近年では予防的な対応を重視する.
特に,苦痛の予防を実現させるための方略として重視するのが,
・疾病の経過(illness trajectory)の把握
・今後起こりうる問題の予測と苦痛への対処
・患者と家族をケアの1単位としてとらえること
・尊厳の尊重と誠実でオープンなコミュニケーション
である38).
緩和ケアの提供には診療報酬上の課題や緩和ケアや認知症に関するスタッフ教育,スタッフの短期間での交代や不適切なコミュニケーションなどのバリアがある13).しかし,現在では緩和ケアの対象はがんから血管疾患,呼吸器疾患,腎疾患,認知症,集中治療などに広がっている.
II.疾病の経過の理解
現在,先進国では,主たる死亡原因が,悪性腫瘍や心疾患,呼吸器疾患,脳血管性障害などの慢性疾患で占められる.
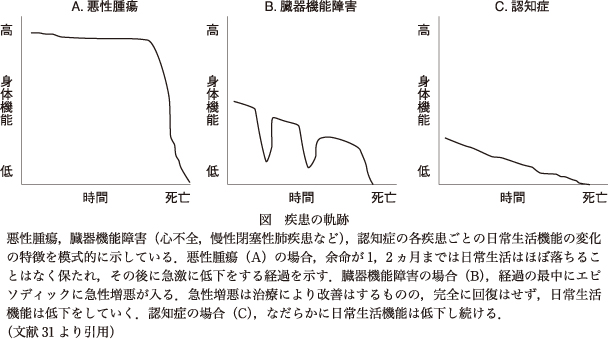
これらの慢性疾患の進行は,大きく3つのパターンに整理できる(図)31).
①比較的長期間機能は保たれ,死亡前,数週間から1,2ヵ月前に身体機能が急激に低下するパターン(典型的には進行期の悪性腫瘍).短期の介護が可能であれば在宅での看取りも可能である.また,認知機能も保たれるため,本人の意思を確認することも比較的容易である.
②心臓や肺などの臓器機能障害が中心に進行する場合には,数ヵ月から数年にわたり,急性増悪と回復を繰り返しながら進行し,最後は比較的急な経過をたどる(慢性心不全や慢性閉塞性肺疾患).急性増悪のときには,治療により改善の可能性はあるものの,回復したとしても以前よりは日常生活機能が低下する.
③機能が低下した状態が数年以上続き,機能がゆるやかに低下する(老衰や認知症).終末期かどうかの判断は難しい.さらにいざ意思決定が必要な場面が生じる事態になると,その時点での本人の意思の確認が難しい場合が多い.
III.認知症に対する緩和ケアのアプローチ
緩和ケアアプローチの特徴は,このような疾病の経過を把握し,対策をたてることにある.
認知症もがんと同様に,確実な治療法がなく,緩徐に進行し,やがて死に至る疾患である42)49)55).認知症の経過は,早期と中期,後期に分けられる50).エンドオブライフにおける身体機能の低下の流れを知ることは,後期認知症に対するケアを検討するうえで役に立つ27).
従来は,終末期というと,医学的に死のプロセスに入ったと見なされる時期からを指していたが,近年のエンドオブライフの概念では,死に明らかにつながる時期以前の高度の機能障害が持続する時期を含む概念に拡張されつつある20).
認知症においてもがんと同様に,患者が疾病のどの時期にいるのかを把握し,治療のゴール設定を繰り返し患者と医療者が話し合うプロセスは可能である27).
認知症が進行するにつれて,身体や精神機能の維持,併存症に伴うさまざまな苦痛の除去も必要となる.さらに,疾病の経過を通じて,患者とその家族の支援ニーズはより具体的になるため,それらを把握し,対応する35).
特にエンドオブライフの段階では,認知症の人の療養中のQOLを落とす要因として,緊急時の入院と効果は不確かで負担を強いる治療,痛みや身体的苦痛への不十分な対応が指摘されている11).
1.認知症と予後
認知症は予後を悪くすることが知られている15)28).
認知症の診断からの生命予後に関して,いくつかのコホート研究が知られており18)32),アジア系では平均4.4年(中央値)であった.注目したいのは,認知症の診断時からの予後はかなり短いこと,多くは認知症の進行によって(重度の認知症に至って)死亡する前に,併存症や合併症により死亡している点39)41)56),コリンエステラーゼ阻害薬の使用による差異は認められていない18)点である.
2.認知症をもつ人への心理的支援
疾患への適応を支援することは,緩和ケアの重要な介入の1つである.特に,患者と医療者が疾病の経過や価値観を共有し,いかに過ごすかを話し合うACPはその中核をなす.認知症の患者は軽度でも,ある程度進行した段階でも,自らの疾患に対して違和感を認識し,苦痛を感じており,苦痛に応じた精神心理的支援が必要である36).従来,本人が認識できないとの先入観から見落とされていたが,重度の認知症のように病識を失った場合でも,目に見える形や具体的な行事を通した支援の可能性がある5)43)48).
1)重要な話し合いをもつこと
認知症やがんの告知のように,患者・家族の今後の見通しを根底から覆すような話題はbad news(悪い知らせ)として知られ,医療者にとっても患者・家族にとっても負担が大きく,気が進まないものである.しかし,医療者と患者・家族が同じ話題を共有することにより,
①孤独感を軽減し,知らないために起こりうる不安や恐怖を軽減する
②患者と家族,介護者の孤立を防ぐ
③患者が自分の意向を伝え,尊重されることを実際に確認することで,医療者や介護者との信頼関係を築く
ことができる11).
実際に,告知や治療に関する話題は,一度にすべてを伝え,決めることは難しい.本人のニーズを踏まえ,情緒的なサポートをしつつ,できる範囲のことから慎重に話を進めていく.
認知症は,情報をまとめ,理解し,処理・判断する能力の低下だけではなく,自分自身の感情などについて説明し伝える力も障害される4).臨床経験から,静かでリラックスできる環境で多めの時間を用意すること,簡単でわかりやすい言葉で説明をすること,アイコンタクトを保ち,返答をゆっくり待つこと,友人や家族のように本人が信頼している人の同席のもとで行うこと,などの工夫が提案されている4).
2)意思決定支援―アドバンス・ケア・プランニング―
生命予後が限られてきた時期において,療養生活や治療の方向性を定め,患者の療養中のQOLを最大化させるための取り組みとして重要になるのがACPである.ACPは,本人が自ら決定をし,希望を表明できなくなった場合に備えて,本人にとって重大な影響を及ぼす可能性のある選択について,時間をかけて検討し,患者と医療者の間で価値観や意向を共有し,治療の目標を設定する試みである10)46).ACPは,療養中のQOLの向上を図るうえで,痛みのマネジメントや抑うつ・不安への対応,悪い知らせを伝え,今後を話し合うコミュニケーション・スキルとあわせて,基本的緩和ケアに含まれる10)38).
一般に,ACPは,終末期における治療や療養場所を話し合う話題として取り上げられることが多い.しかし,認知症の場合は,生命や身体にかかわるような重要な決定をする能力が保たれている早期の段階で,実施することが望まれる.
主たる話し合いの内容には,療養場所に関する意向や積極的な治療に関する希望,栄養や補液についての希望,体調を崩した際の入院の希望など,中長期的な視点での介護・ケアに関するものも含まれる13).
ACPを認知症の人に対して実施することにより,苦痛の緩和やケアへの満足度が高まったとの報告がある11).多くの報告はケアホームで,進行期の段階での議論も含まれており,ケアホームなど長期のケア施設にとどまる選択がなされる.疾病の早期の段階でACPを始めることについては,まだエビデンスは乏しい.しかし,海外においては,より早期の段階でACPを実施することにより,不必要な入院を回避したり,死の直前にICUで治療を受ける割合が有意に低下し,最終的にコストも低下したとの報告がある37).
3.認知症と身体機能,合併症
認知症の人は,一般的に老年症候群を合併することが多い34).認知症の人の快適さを最大限に維持するためにも,身体機能の低下を防ぐ取り組みが重要になる.一方で,併存症を発症した場合に,その効果が不確実で,かつ過剰な侵襲や過剰な負担を強いることは避けなければならない47).しかし,現実には,併存症の発症が,進行期の認知症のエンドオブライフであることが認識されていない.その結果,一貫したマネジメントがなされないため,過負荷を強いる対応(例えば,緊急入院や経静脈的な抗菌薬の投与,胃管の留置など)が見通しを検討されないまま実施されている現状がある.
進行期の認知症に併存し,一般に死に至る要因となるものに,肺炎と感染,食事の問題がある34).
QOLを考えるうえで,療養場所は大きな比重を占める要因である.特に入院治療は,通常エンドオブライフの質を考えると推奨される場所ではないが,現実には海外においても合併症とそれに伴う長期入院の末,進行期の認知症の20%が病院で死を迎えている33)47).しかし,経時的な経過をみると,介護施設に入所していた患者が入院すると,ホスピス・緩和ケア病棟を勧められる割合が高まってきているとの報告がある2).これは,認知症を含めた高齢者のエンドオブライフ・ケアにおけるホスピス・緩和ケア病棟が,緊急入院や病院死を防ぐとともに,エンドオブライフにおけるケアの断絶を防止して,療養中のQOLの向上に資する役割が確立しつつあることも1つの要因である.
わが国においては,診療報酬上,ホスピス・緩和ケア病棟の対象が,悪性腫瘍の患者または後天性免疫不全症候群に罹患している患者に制限されている現状がある29).わが国においては,介護施設と病院の間を補完する方法が求められる.
1)感染
感染症は認知症の経過に含まれるイベントであるが,急性期病院に入院を促進させる要因でもある.特に,脱水と感染で入院を繰り返すことは,生命予後が短いことと関連する3).Nursing homeに入所している認知症患者の前向き観察研究では,66%が何らかの感染症に罹患し,平均2.5回の医療的介入が行われていた(移送など).これらの処置は,次回感染などの問題が生じた際の入院の是非などの話し合いがない場合に多かった.
認知症患者では,肺炎と尿路感染が高頻度に合併する.上記の観察研究でも,感染が疑われた患者のうち72%に抗菌薬が使用されていた3).抗菌薬による治療は,症状を改善させるものの,感染自体を繰り返すことが本人・家族に対して負担となる.多剤耐性菌が広まり,その対応は進行期の認知症ケアでは問題になっている.尿路感染に対する抗菌薬の使用に関する観察研究では,抗菌薬の使用が生存率の向上に寄与しなかったことも指摘されている12).一般病院とnursing homeで肺炎治療をした場合を比較した検討では,一般病院での治療のほうが生命予後は長かった一方,環境や機能的な面では悪く,総合アウトカムでは劣っていた21)30).
2)低栄養
食事の摂取の問題は,終末期の問題に気づく契機になる.
終末期では,自力での摂食が困難になることに加えて,食事の拒否や嚥下障害,誤嚥性肺炎など食事に絡んだ問題が増加する.食事の問題が生じた進行期認知症の人の6ヵ月後の生存率は39%であった34).しかし,食事に絡んだ問題が生じていたとしても,介護者は経管栄養を選択すべきかどうかに直面すると困難を感じる.経管栄養を終末期に実施すると,生命予後の延長は期待しづらい一方,処置に伴う抵抗や褥瘡の発症,医療対応の増加や身体抑制の増加につながることから,用手的な介助が推奨されている1).
4.認知症の行動・心理症状(BPSD)と身体症状
認知症の人の身体症状は,常に過小診断と過小治療の危険があり,特に痛みや呼吸困難の評価の必要性が指摘されている8)34).
BPSDを疑う場合も,身体症状とあわせて対処される必要がある.例えば,疼痛緩和を図ることで興奮を抑えることがあり,また抑うつ症状や身体活動の変化が興奮に影響することもある44)51).
5.痛みへの対応の必要性
痛みの管理は,認知症の人にとって,非常に重要な支援である.特に重度の認知症の場合には,非言語的な行動を注意深く観察することが重要である.
痛みは客観的な評価が難しく,また認知症に伴う神経生理学的変化や認知機能障害が重なり,主観的にも評価が難しくなる.両者の影響により,痛みが医療従事者や介護者に認識されず,対応されない事態を招く.これは,認知症が重度になるほど多くなるともいわれる9)14).
実際に臨床では,信頼性は落ちるものの,まず患者の自己評価を求めることから始める.軽度および中等度の認知症の場合には,疼痛評価に自己評価法を利用することができる.しかし,進行した認知症の場合は自己評価が困難となり,身振りや顔つきを手がかりとして対応せざるを得ない26).認知症の痛みの評価に関してはこれまでにさまざまなツールが開発されている.代表的な客観的評価尺度に,Pain Assessment in Advanced Dementia(PAINAD)ScaleおよびDoloplusなどがある24)25)53)54)58)59).
IV.認知症の経過と家族への支援
認知症の診断と予後の話し合いは,今後の患者・家族のニーズを推測し対応するために重要であるが,難しい課題でもある19).特に家族の抑うつは,療養場所の検討をするうえで重要な要因であり,話し合いとあわせて支援が求められる.
急なイベントが起きた際にも,適切な支援を受けることにより,介護者はより早期の場合でも今後の経過を踏まえた選択を示すことができる.近年では,ビデオなどの意思決定支援ツールを用いた支援の効果を検討した報告もあり,より広範な話し合いを事前にすることにより,入院を避けることを支援することが可能かもしれない22).
1.家族教育の必要性
認知症の経過と関連する健康上の問題について,家族の多くはほとんど理解していない6)19).病気の状態や患者の世界について,継続的に教育的にかかわることは,家族支援として有用である.情報は,その都度,段階を踏んで提供する16)52).
特に,認知症の進行に伴い,家族は意思決定の共有あるいは代理をせざるを得なくなることを事前に知り,あらかじめ心構えをもつことは,QOLを高めるために重要である23).
2.悲嘆への支援
数年にわたり認知症の人の支援を続けてきた介護者の悲嘆反応は,複雑で遷延しやすい.介護に携わる期間が年単位と長期であるにもかかわらず,約4人に1人の介護者は,死への備えをしていなかったとの報告がある23).死別反応は,認知症の人の死から始まるが,多くの場合,悲嘆のプロセス自体は,認知症の診断のときから始まる17).
予期悲嘆は,まだ存命の人を今後喪うことに対する嘆きである.認知症では,軽度認知機能障害や認知症が明らかになった時点から生じる.予期悲嘆は介護者の47~71%に生じる7).また,悲嘆が複雑・遷延化する複雑性悲嘆は死別後の介護者のうち,20%に起こるとの報告がある45).複雑性悲嘆は,介護者が抑うつ状態であったことや認知症の人の機能障害がより重度であったことと関連した.介護者に対する心理社会的な支援は,複雑性悲嘆の発症を低下させた.
おわりに
認知症では身体合併症を併存することが非常に多い.身体治療とケアを進めるうえで,緩和ケアのアプローチは,患者・家族の支援の全体像を示すことができ有用である.
高齢者ケアの課題は,わが国が世界に先駆けて直面している課題であり,世界に向けて貢献できる領域でもある.精神医学と緩和ケアの連携がより進むことを願っている.
なお,本論文に関連して開示すべき利益相反はない.
1) American Geriatrics Society Ethics Committee and Clinical Practice and Models of Care Committee: American Geriatrics Society feeding tubes in advanced dementia position statement. J Am Geriatr Soc, 62 (8); 1590-1593, 2014![]()
2) Ankuda, C. K., Mitchell, S. L., Gozalo, P., et al.: Association of Physician Specialty with Hospice Referral for Hospitalized Nursing Home Patients with Advanced Dementia. J Am Geriatr Soc, 65 (8); 1784-1788, 2017![]()
3) Boeve, B. F., Silber, M. H., Parisi, J. E., et al.: Synucleinopathy pathology and REM sleep behavior disorder plus dementia or parkinsonism. Neurology, 61 (1); 40-45, 2003![]()
4) British Medical Association: Assessment of mental capacity, guidance for doctors and lawyers. BMA Books, London, 1995
5) Buckwalter, G. L.: Addressing the spiritual & religious needs of persons with profound memory loss. Home Healthc Nurse, 21 (1); 20-24, 2003![]()
6) Caron, C. D., Griffith, J., Arcand, M.: Decision making at the end of life in dementia: how family caregivers perceive their interactions with health care providers in long-term care settings. Journal of Applied Gerontology, 24; 231-247, 2005
7) Chan, D., Livingston, G., Jones, L., et al.: Grief reactions in dementia carers: a systematic review. Int J Geriatr Psychiatry, 28 (1); 1-17, 2013![]()
8) Chibnall, J. T., Tait, R. C., Harman, B., et al.: Effect of acetaminophen on behavior, well-being, and psychotropic medication use in nursing home residents with moderate-to-severe dementia. J Am Geriatr Soc, 53 (11); 1921-1929, 2005![]()
9) Cohen-Mansfield, J.: The adequacy of the minimum data set assessment of pain in cognitively impaired nursing home residents. J Pain Symptom Manage, 27 (4); 343-351, 2004![]()
10) Committee on Approaching Death: Addressing Key End of Life Issues, Institute of Medicine: Dying in America: Improving Quality and Honoring Individual Preferences Near the End of Life. National Academies of Sciences Engineering Medicine, Washington, D. C., 2015
11) Dixon, J., Karagiannidou, M., Knapp, M.: The Effectiveness of Advance Care Planning in Improving End-of-Life Outcomes for People With Dementia and Their Carers: A Systematic Review and Critical Discussion. J Pain Symptom Manage, 55 (1); 132-150 e1, 2018![]()
12) Dufour, A. B., Shaffer, M. L., D'Agata, E. M., et al.: Survival After Suspected Urinary Tract Infection in Individuals with Advanced Dementia. J Am Geriatr Soc, 63 (12); 2472-2477, 2015![]()
13) Erel, M., Marcus, E. L., Dekeyser-Ganz, F.: Barriers to palliative care for advanced dementia: a scoping review. Ann Palliat Med, 6 (4); 365-379, 2017![]()
14) Fisher, S. E., Burgio, L. D., Thorn, B. E., et al.: Pain assessment and management in cognitively impaired nursing home residents: association of certified nursing assistant pain report, Minimum Data Set pain report, and analgesic medication use. J Am Geriatr Soc, 50 (1); 152-156, 2002![]()
15) Fitzpatrick, A. L., Kuller, L. H., Lopez, O. L., et al.: Survival following dementia onset: Alzheimer's disease and vascular dementia. J Neurol Sci, 229-230; 43-49, 2005![]()
16) Fried, T. R., Redding, C. A., Robbins, M. L., et al.: Stages of change for the component behaviors of advance care planning. J Am Geriatr Soc, 58 (12); 2329-2336, 2010![]()
17) Garand, L., Lingler, J. H., Deardorf, K. E., et al.: Anticipatory grief in new family caregivers of persons with mild cognitive impairment and dementia. Alzheimer Dis Assoc Disord, 26 (2); 159-165, 2012![]()
18) Garcia-Ptacek, S., Farahmand, B., Kåreholt, I., et al.: Mortality risk after dementia diagnosis by dementia type and underlying factors: a cohort of 15,209 patients based on the Swedish Dementia Registry. J Alzheimers Dis, 41 (2); 467-477, 2014![]()
19) Gessert, C. E., Forbes, S., Bern-Klug, M.: Planning end-of-life care for patients with dementia: roles of families and health professionals. Omega (Westport), 42 (4); 273-291, 2000![]()
20) Gill, T. M., Gahbauer, E. A., Han, L., et al.: Trajectories of disability in the last year of life. N Engl J Med, 362 (13); 1173-1180, 2010![]()
21) Givens, J. L., Jones, R. N., Shaffer, M. L., et al.: Survival and comfort after treatment of pneumonia in advanced dementia. Arch Intern Med, 170 (13); 1102-1107, 2010![]()
22) Hanson, L. C., Zimmerman, S., Song, M. K., et al.: Effect of the Goals of Care Intervention for Advanced Dementia: A Randomized Clinical Trial. JAMA Intern Med, 177 (1); 24-31, 2017![]()
23) Hebert, R. S., Dang, Q., Schulz, R.: Preparedness for the death of a loved one and mental health in bereaved caregivers of patients with dementia: findings from the REACH study. J Palliat Med, 9 (3); 683-693, 2006![]()
24) Herr, K., Bjoro, K., Decker, S.: Tools for assessment of pain in nonverbal older adults with dementia: a state-of-the-science review. J Pain Symptom Manage, 31 (2); 170-192, 2006![]()
25) Herr, K., Coyne, P. J., Key, T., et al.: Pain assessment in the nonverbal patient: position statement with clinical practice recommendations. Pain Manag Nurs, 7 (2); 44-52, 2006![]()
26) Horgas, A. L., Elliott, A. F., Marsiske, M.: Pain assessment in persons with dementia: relationship between self-report and behavioral observation. J Am Geriatr Soc, 57 (1); 126-132, 2009![]()
27) Kiely, D. K., Givens, J. L., Shaffer, M. L., et al.: Hospice use and outcomes in nursing home residents with advanced dementia. J Am Geriatr Soc, 58 (12); 2284-2291, 2010![]()
28) Knopman, D. S., Parisi, J. E., Boeve, B. F., et al.: Vascular dementia in a population-based autopsy study. Arch Neurol, 60 (4); 569-575, 2003![]()
29) 厚生労働省: 平成30年3月5日保医発0305第2号: 基本診療料の施設基準等及びその届出に関する手続きの取扱いについて(通知)「第14緩和ケア病棟入院料」. 2018 (https://www.mhlw.go.jp/file/06-Seisakujouhou-12400000-Hokenkyoku/0000205633.pdf)(参照2019-01-24)
30) Loeb, M., Carusone, S. C., Goeree, R., et al.: Effect of a clinical pathway to reduce hospitalizations in nursing home residents with pneumonia: a randomized controlled trial. JAMA, 295 (21); 2503-2510, 2006![]()
31) Lunney, J. R., Lynn, J., Foley, D. J., et al.: Patterns of functional decline at the end of life. JAMA, 289 (18); 2387-2392, 2003![]()
32) Mayeda, E. R., Glymour, M. M., Quesenberry, C. P., et al.: Survival after dementia diagnosis in five racial/ethnic groups. Alzheimers Dement, 13 (7); 761-769, 2017![]()
33) Mitchell, S. L., Teno, J. M., Miller, S. C., et al.: A national study of the location of death for older persons with dementia. J Am Geriatr Soc, 53 (2); 299-305, 2005![]()
34) Mitchell, S. L., Teno, J. M., Kiely, D. K., et al.: The clinical course of advanced dementia. N Engl J Med, 361 (16); 1529-1538, 2009![]()
35) Mohamed, S., Rosenheck, R., Lyketsos, C. G., et al.: Caregiver burden in Alzheimer disease: cross-sectional and longitudinal patient correlates. Am J Geriatr Psychiatry, 18 (10); 917-927, 2010![]()
36) Nelis, S. M., Clare, L., Martyr, A., et al.: Awareness of social and emotional functioning in people with early-stage dementia and implications for carers. Aging Ment Health, 15 (8); 961-969, 2011![]()
37) Nicholas, L. H., Bynum, J. P., Iwashyna, T. J., et al.: Advance directives and nursing home stays associated with less aggressive end-of-life care for patients with severe dementia. Health Aff (Millwood), 33 (4); 667-674, 2014![]()
38) 日本医師会: 新版がん緩和ケアガイドブック. 青海社, 東京, 2017
39) Oesterhus, R., Soennesyn, H., Rongve, A., et al.: Long-term mortality in a cohort of home-dwelling elderly with mild Alzheimer's disease and Lewy body dementia. Dement Geriatr Cogn Disord, 38 (3―4); 161-169, 2014![]()
40) 小川朝生: 認知症の緩和ケア. 精神経誌, 118 (11); 813-822, 2016
41) Onyike, C. U., Diehl-Schmid, J.: The epidemiology of frontotemporal dementia. Int Rev Psychiatry, 25 (2); 130-137, 2013![]()
42) Radbruch, L, Payne, S.: White paper on standards and norms for hospice and palliative care in Europe: part 1 Recommendation from the European Association for Palliative Care. European Journal of Palliative Care, 16 (6); 278-289, 2009
43) Sampson, E. L., Gould, V., Lee, D., et al.: Differences in care received by patients with and without dementia who died during acute hospital admission: a retrospective case note study. Age Ageing, 35 (2); 187-189, 2006![]()
44) Scherder, E. J., Bogen, T., Eggermont, L. H., et al.: The more physical inactivity, the more agitation in dementia. Int Psychogeriatr, 22 (8); 1203-1208, 2010![]()
45) Schulz, R., Boerner, K., Shear, K., et al.: Predictors of complicated grief among dementia caregivers: a prospective study of bereavement. Am J Geriatr Psychiatry, 14 (8); 650-658, 2006![]()
46) Sudore, R. L., Lum, H. D., You, J. J., et al.: Defining Advance Care Planning for Adults: A Consensus Definition From a Multidisciplinary Delphi Panel. J Pain Symptom Manage, 53 (5); 821-832e1, 2017![]()
47) Teno, J. M., Gozalo, P. L., Bynum, J. P., et al.: Change in end-of-life care for Medicare beneficiaries: site of death, place of care, and health care transitions in 2000, 2005, and 2009. JAMA, 309 (5); 470-477, 2013![]()
48) Tilly, J., Abel, F.: Quality end of life care for individuals with dementia in assisted living and nursing homes and public policy barriers to delivering this care. US Alzheimer's Association, 2007 (https://www.alz.org/documents/national/End_interviewpaper_III.pdf) (参照2019-01-24)
49) van der Steen, J. T.: Dying with dementia: what we know after more than a decade of research. J Alzheimers Dis, 22 (1); 37-55, 2010![]()
50) van der Steen, J. T., Radbruch, L., Hertogh, C. M., et al.: White paper defining optimal palliative care in older people with dementia: a Delphi study and recommendations from the European Association for Palliative Care. Palliat Med, 28 (3); 197-209, 2014![]()
51) Volicer, L., Frijters, D. H., van, der, Steen, J. T.: Relationship between symptoms of depression and agitation in nursing home residents with dementia. Int J Geriatr Psychiatry, 27 (7); 749-754, 2012![]()
52) Wald, C., Fahy, M., Walker, Z., et al.: What to tell dementia caregivers: the rule of threes. Int J Geriatr Psychiatry, 18 (4); 313-317, 2003![]()
53) Warden, V., Hurley, A. C., Volicer, L.: Development and psychometric evaluation of the Pain Assessment in Advanced Dementia (PAINAD) scale. J Am Med Dir Assoc, 4 (1); 9-15, 2003![]()
54) Wary, B., Doloplus, C.: [Doloplus-2, a scale for pain measurement]. Soins Gerontol, (19); 25-27, 1999
55) Wolf-Klein, G., Pekmezaris, R., Chin, L., et al.: Conceptualizing Alzheimer's disease as a terminal medical illness. Am J Hosp Palliat Care, 24 (1); 77-82, 2007![]()
56) Wolfson, C., Wolfson, D. B., Asgharian, M., et al.: A reevaluation of the duration of survival after the onset of dementia. N Engl J Med, 344 (15); 1111-1116, 2001![]()
57) World Organization of Health: WHO Definition of Palliative Care (https://www.who.int/cancer/palliative/definition/en/)〔緩和ケア関連団体会議定訳 (http://www.jspm.ne.jp/proposal/proposal.html)〕(参照2019-01-24)
58) Zwakhalen, S. M., Hamers, J. P., Abu-Saad, H. H., et al.: Pain in elderly people with severe dementia: a systematic review of behavioural pain assessment tools. BMC Geriatr, 6; 3, 2006![]()
59) Zwakhalen, S. M., Hamers, J. P., Berger, M. P.: The psychometric quality and clinical usefulness of three pain assessment tools for elderly people with dementia. Pain, 126 (1-3); 210-220, 2006![]()