われわれは,カルボニルストレス抑制薬であるピリドキサミンの効果を検証する目的で,医師主導型治験を実施した.対象は,カルボニルストレスが亢進している統合失調症患者10名で,代表的なカルボニルストレスバイオマーカーである血漿ペントシジン値を用いて被験者をリクルートした.単群非盲検のデザインで,24週間かけて実施し,有効性評価は,Positive and Negative Syndrome Scale(PANSS)スコアおよびBrief Psychiatric Rating Scale(BPRS)スコアの治験前後での変化量とした.また,安全性については薬剤性錐体外路症状をDrug Induced Extra-Pyramidal Symptoms Scale(DIEPSS)で,自殺関連症状をColumbia-Suicide Severity Rating Scale(C-SSRS)でそれぞれ評価した.10名のうち2名はPANSSで顕著な改善を認めた.遺伝的にカルボニルストレス脆弱性を有する被験者はペントシジンの大幅な減少を認めると同時に,PANSSの中等度改善を認めた.DIEPSSでは,4名の患者で20%以上の改善を認めた.自殺に関する有害事象は生じなかったが,2名において,重大な副作用であるウェルニッケ様脳症が発生した.いずれの被験者もチアミンの速やかな投与により後遺症なく回復した.
2)東京都立松沢病院精神科
3)東京都立大塚病院神経科
はじめに
カルボニルストレスの亢進とは,反応性に富む有害なカルボニル化合物が生体内で蓄積することであり,カルボニル化合物の産生過多あるいは解毒代謝回路の破綻によって引き起こされる22).カルボニルストレスが亢進すると,終末糖化産物(advanced glycation end products:AGEs)が蓄積する.AGEsは糖尿病7)17)24),腎機能障害22),心血管障害12)などの病態に深く関与することが知られている.一方,3種類存在するビタミンB6のうち,ピリドキサミンはカルボニル化合物を捕捉することでAGEsの産生を抑制し,カルボニルストレス抑制作用を発揮する.他の2種類のビタミンB6(ピリドキシン,ピリドキサール)にはカルボニルストレス緩和作用はない.
われわれは,統合失調症患者の約20%で,代表的なAGEsであるペントシジンが蓄積し,ビタミンB6が枯渇するというカルボニルストレスの亢進が生じることを明らかにし3),異なる患者集団で再現性も確認してきた19).また,カルボニルストレスが亢進した統合失調症患者の臨床症状・経過を精査した結果,長期入院,大量の抗精神病薬内服という治療抵抗性統合失調症に類似した臨床特徴を抽出し,血清ビタミンB6濃度が精神症状と負に相関することも見出した20).今日まで,クロザピンが治療抵抗性統合失調症に対する唯一の治療薬であるが16)18),顆粒球減少などの致死的副作用を防ぐために頻回の採血を要するなど負担が大きい1).そこでわれわれは,カルボニルストレスが亢進した治療抵抗性類似の統合失調症患者に対して,カルボニルストレス抑制作用を有するピリドキサミンが新しい安全な治療薬となる可能性を検証するために,東京都立松沢病院において医師主導型治験を実施した10).
I.研究の方法および結果
1.対象者
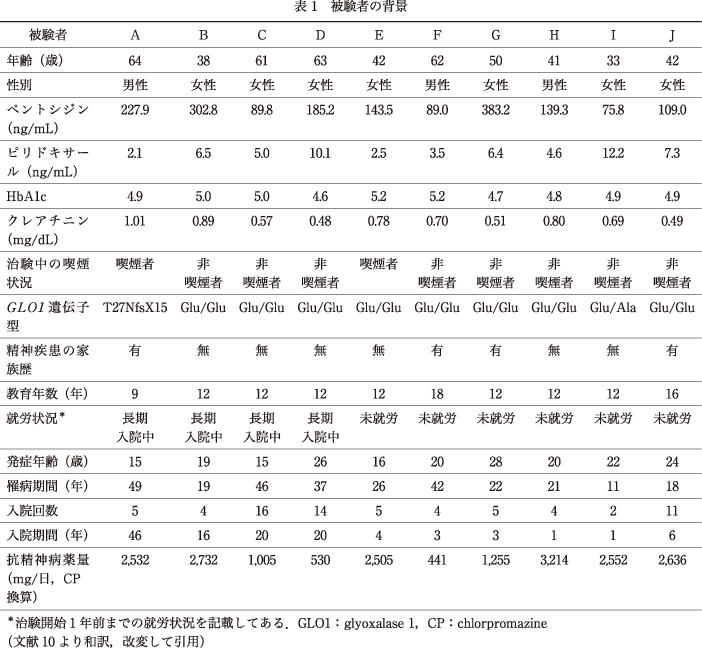
東京都立松沢病院に入院中の20~65歳までの患者で,DSM-IVによる統合失調症あるいは統合失調感情障害の診断基準を満たしたものを対象とした.また,カルボニルストレス亢進のバイオマーカーとして血漿ペントシジン値を採用し,先行研究から算出された高値(55.2 ng/mL)を示す患者を治験に組み入れた.ペントシジン値に影響する糖尿病や腎機能障害の合併,5年以内の悪性腫瘍の既往,試験開始直近の修正型電気けいれん療法の既往を有する患者は除外した.ペントシジン値に加えて,ビタミンB6値も選択基準に組み込むことが期待されたが,ペントシジン高値なおかつビタミンB6低値を呈する患者が極端に少ないため,今回はペントシジン値のみをリクルート基準に採用した.
2.試験デザイン
24週,単群非盲検のデザインとし,治験前から内服している抗精神病薬は原則として用法・用量を変更せず継続した.ピリドキサミンは1,200 mg/日,1,800 mg/日および2,400 mg/日の3用量を設定し,1日3回に分けて内服することとした.必ず1,200 mg/日から開始し,増量の可否は試験担当医師によって判断された.治験のプロトコールは東京都立松沢病院の治験審査委員会で承認され,すべての患者からインフォームドコンセントを得たうえで実施した(臨床試験登録番号:UMIN000006398).
3.有効性・安全性評価
試験前後のPositive and Negative Syndrome Scale(PANSS)およびBrief Psychiatric Rating Scale(BPRS)スコアの変化量を有効性の主要評価項目とした.また,安全性評価項目として,Drug Induced Extra-Pyramidal Symptoms Scale(DIEPSS)およびColumbia-Suicide Severity Rating Scale(C-SSRS)を実施した.バイタルサイン,有害事象出現の有無を注意深く観察し,血液検査や心電図を定期的に実施して被験者の安全の確保に努めた.
4.カルボニルストレス関連バイオマーカーの測定
血漿ペントシジン値は先行研究と同様にHPLCを用いて測定した21).3種類の血清ビタミンB6は株式会社エスアールエルおよび株式会社LSIメディエンスに委託して測定した.カルボニル化合物の解毒回路を構成する主要な酵素にglyoxalase 1(GLO1)がある.すべての被験者でGLO1遺伝子型を特定し,カルボニルストレスに対する遺伝的脆弱性を確認した.
5.結 果
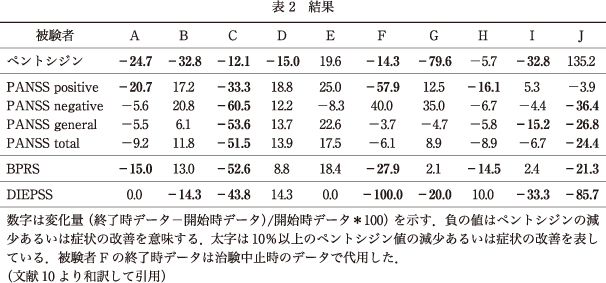
被験者の背景を表1にまとめた.10名の被験者のうち,4名は長期入院中であった.治験の結果を表2に示す.10名中1名(被験者F)は,全身状態悪化のため121日目に試験から脱落しており,9名の患者が治験を完遂した.そのうち2名でPANSSおよびBPRSの顕著な改善を認めた.この2名は疎通性,感情表出が明らかに改善し,作業療法への参加率が上昇した.さらに,うち1名は試験開始前には独歩できなかったが,リハビリ意欲が改善したこともあり,終了時には独歩可能となった.このような劇的な改善は過去にはまったく観察されていないことであり,スタッフも驚きの声を上げるほどであった.残念ながら,独歩可能となった被験者は,治験終了後にピリドキサミン投与をやめると治験前の精神状態にまで悪化した.GLO1遺伝子に稀なフレームシフト変異を有する被験者では,血漿ペントシジンが25%減少すると同時に,PANSS,BPRSの中等度の改善を認めた.また,興味深いことに4名の患者でDIEPSSが20%以上改善した.脱落した被験者Fに確認されたDIEPSSの大幅な改善は,全身状態悪化による抗精神病薬の中止の影響であった.
血漿ペントシジン値は治験全体で26.8%の減少を認めた.通常,血漿ペントシジンは安定した物質であり,53名の統合失調症入院患者を108日間追跡した場合では,わずか3%の変化にとどまっている11).以上を考慮すれば,本治験ではピリドキサミンによる明らかなカルボニルストレス抑制効果を認めたと考えられる.
本治験で生じた副作用および因果関係が否定できない有害事象を表3にまとめた.重大な副作用として,ウェルニッケ様脳症が2名に生じたが,いずれも迅速なチアミンの投与により後遺症なく回復している.本副作用の発生以後は,ビタミンB1を併用する治験プロトコールに修正し,あらためて全被験者にインフォームドコンセントを得たうえで治験を継続した.
II.考察―本論文の意義,苦労・工夫したことなどを含めて―
1.考 察
今回の治験では,カルボニルストレスが亢進している統合失調症患者に対して,カルボニルストレス抑制作用を有するピリドキサミンの効果および安全性を検証した.その結果,2名の患者で精神症状が劇的に改善し,カルボニルストレスへの遺伝的な脆弱性を有する患者では,ペントシジン値が減少するとともに,中等度の精神症状の改善を認めた10).また,薬剤性錐体外路症状の改善を4名の患者で認めたが,重大な副作用としてウェルニッケ様脳症が2名に生じた10).
今回の治験では,全例でペントシジンの減少を認めたわけではない.特に,精神症状が著しく改善した被験者2名のうち1名はペントシジンが大幅に増加した.したがって,ピリドキサミンには,カルボニルストレス抑制作用とは異なる効果発現の機序が存在する.例えば,glutamic acid decarboxylase(GAD)やaromatic L-amino acid decarboxylaseはピリドキサール依存性である.ピリドキサミンから変換されたピリドキサールによって,ドパミン,セロトニンやγ-アミノ酪酸(γ-aminobutyric acid:GABA)などの神経伝達物質が調整され,精神症状の改善に関与したかもしれない.実際,マウスではピリドキシン投与によって,海馬での脳由来神経栄養因子(brain-derived neurotrophic factor:BDNF)の有意な上昇や,海馬歯状回におけるGAD蛋白の発現上昇などの報告がある28)29).推察ではあるが,副作用としてみられた過鎮静はGABA濃度の変化に起因するかもしれないし,著効例に認められた陰性症状や日中の活動性の改善,そして薬剤性錐体外路症状の改善などは,セロトニンやドパミン系への影響かもしれない.
結果の項目でも言及したが,大量のピリドキサミン投与によってウェルニッケ様脳症が2例発生した.過去の報告によれば,大量のピリドキサールを投与されたマウスはけいれんによって死に至ることがある.またヒトでは,大量のピリドキシンが末梢神経炎に関連した神経毒性を惹起したり5)26),慢性期の統合失調症患者ではめまいを生じたりすること2)が報告されているものの,ウェルニッケ様脳症の発生に関する報告はない.ウェルニッケ様脳症をきたしたメカニズムとして,投与された大量のピリドキサミンがピリドキサールに変換され,アミノ基を有するチアミンを捕捉して枯渇させた可能性が高いと推察される.しかしながら,8週齢のC57BL/6Jマウス(4~8匹)に30 mg/kg/日,100 mg/kg/日および500 mg/kg/日のピリドキサミンを経口ゾンデにより30日間投与したが,ウェルニッケ様脳症を再現する所見は認められず,正確な発症機序は不明である.全例にチアミンを併用するプロトコールに変更してからウェルニッケ様脳症は発生しておらず,十分に予防可能な副作用と考えられる.
2.意 義
1973年以降,いくつかの研究でビタミンB6の統合失調症に対する有効性が報告されている2)4)6)13-15)25)が,いずれも当然のことながらカルボニルストレス抑制仮説に沿ったものではない.したがって,各試験で使用されたビタミンB6はピリドキサミンではなく,ピリドキシンやピリドキサールといった他のビタミンB6が用いられている.また,結果はそれぞれの研究間で一致していない.本治験が非常にユニークである点は,カルボニルストレス亢進仮説に則り,カルボニルストレスバイオマーカーで被験者をリクルートし,カルボニルストレス抑制薬の効果を検証した点にある.その結果,遺伝的にカルボニルストレス脆弱性を有する1例では,ペントシジンの減少と同時に精神症状の中等度以上の改善を認めた.このことは,カルボニルストレスが緩和されることによって精神症状が改善する患者が存在することを示しており,とりもなおさずカルボニルストレスが病態に深く関与する統合失調症のサブタイプがある可能性を示唆している.
ペントシジンは通常安定した化合物であるが治験全体を通じて26.8%も減少している.AGEsはAGEs受容体(receptor for AGEs:RAGE)と結合し,細胞内の炎症反応を促進させることが知られており,先に述べた通り糖尿病や心血管障害などさまざまな疾患の病態に関連する.統合失調症は糖尿病や心血管障害による死亡率が健常人と比較して3倍も高く23),平均寿命は20年以上も短い27).ピリドキサミンと身体疾患との関連については,未検証の課題は多いものの,統合失調症の健康問題を考えたときに,ピリドキサミンが貢献できる余地があるかもしれない.
統合失調症の治療薬開発ではproof of concept(POC)が取得されても被験者規模を拡大したRCTで失敗が繰り返され,多くの大手製薬企業が開発から撤退している.ゲノム研究でも有意な関連を示す多型は第一報告が比較的大きなオッズ比を示し,追試やメタ解析ではそれより小さいオッズ比しか得られないことが多い.統合失調症が症候群であるため,サンプリングバイアスが生じやすいこと,POCが獲得できた被験者群と同等の病態をもった集団を再現する方法がないことが治験とゲノム研究のデータで再現性の確保を困難にしている可能性が考えられる8)9).本治験では,カルボニルストレスのバイオマーカーを用いて生化学的病態が比較的均一な集団を抽出し,カルボニルスカベンジャーを投与することで上記の問題を解決できた可能性が示唆される.今後の治療薬開発とゲノム研究の再現性を確保する方向性を示している点で意義があると考える.
3.苦労・工夫したこと
本治験はリクルート基準にカルボニルストレスバイオマーカーであるペントシジン値を組み込んでおり,治験開始前にペントシジンの血漿中濃度を確認する必要がある.とはいえ,基準を満たさない候補者も多く,当初の想定通りにリクルートできない難しさもあったが,ペントシジンが高い統合失調症の臨床特徴である,長期入院中で抗精神病薬内服量が多い比較的症状の重い患者にフォーカスすることで,何とか10名の被験者をリクルートすることができた.ペントシジンが疾患特異性だけではなく,臨床特徴も反映するバイオマーカーであったことは,被験者の組み入れに有用であった.
おわりに―今後の課題および方向性―
今回の治験はピリドキサミンの有効性と安全性を探索的に検証した単群非盲検のデザインである.したがって,ピリドキサミンの有効性を確立するためには,プラセボを用いた二重盲検試験を行う必要があることは言うまでもない.現在,第II相bに相当する治験が進行中であり,結果が待たれる.
カルボニルストレスが統合失調症の発症や病態に与える影響について,順調に基礎研究が進んでいるが不明瞭な部分も大きい.また,考察でも述べたが,カルボニルストレスの減少と症状の改善が必ずしも一致しない被験者がおり,カルボニルストレス仮説では捉えきれない未解明の分子機序についても検討が必要である.カルボニルストレスの疾患への関与,およびピリドキサミンの効果を分子レベルで明らかにするためには,さらなる基礎研究の進展が必要と考えられる.
本研究は,JSPS科研費JP16H05380,JP25861040,JP25253074の支援を受けた.また,本治験データは,16dm0107088h0001,17dm0107088h0002が一部を助成している第II相b治験に活用されている.
本論文はPCN誌に掲載された最新の研究論文10)を編集委員会の依頼により,著者の1人が日本語で書き改め,その意義と展望などにつき加筆したものである.
利益相反
開示すべき利益相反状態にある企業・組織または団体
研究費・助成金など
宮下光弘:株式会社レナサイエンス,興和株式会社
鈴木一浩:興和株式会社
堀内泰江:興和株式会社
鳥海和也:興和株式会社
小堀晶子:興和株式会社
糸川昌成:株式会社レナサイエンス,興和株式会社
新井 誠:株式会社レナサイエンス,興和株式会社
他の著者に開示すべき利益相反はない.
謝 辞 この研究に参加していただいた被験者の皆さんとご家族の方々,そして治験にかかわっていただいたすべての方々に,こころから感謝を申し上げます.
1) Alvir, J. M., Lieberman, J. A., Safferman, A. Z., et al.: Clozapine-induced agranulocytosis. Incidence and risk factors in the United States. N Engl J Med, 329; 162-167, 1993![]()
2) Ananth, J. V., Ban, T. A., Lehmann, H. E.: Potentiation of therapeutic effects of nicotinic acid by pyridoxine in chronic schizophrenics. Can Psychiatr Assoc J, 18; 377-383, 1973![]()
3) Arai, M., Yuzawa, H., Nohara, I., et al.: Enhanced carbonyl stress in a subpopulation of schizophrenia. Arch Gen Psychiatry, 67; 589-597, 2010![]()
4) Ban, T. A., Lehmann, H. E., Deutsch, M.: Negative findings with megavitamins in schizophrenic patients: preliminary report. Commun Psychopharmacol, 1; 119-122, 1977![]()
5) Berger, A. R., Schaumburg, H. H., Schroeder, C., et al.: Dose response, coasting, and differential fiber vulnerability in human toxic neuropathy: a prospective study of pyridoxine neurotoxicity. Neurology, 42; 1367-1370, 1992![]()
6) Bucci, L.: Pyridoxine and schizophrenia. Br J Psychiatry, 122; 240, 1973![]()
7) Hanssen, N. M., Beulens, J. W., van Dieren, S., et al.: Plasma advanced glycation end products are associated with incident cardiovascular events in individuals with type 2 diabetes:a case-cohort study with a median follow-up of 10 years (EPIC-NL). Diabetes, 64; 257-265, 2015![]()
8) 糸川昌成, 新井 誠, 針間博彦ほか: 生物学と統合失調症―物質と物質でないもの―. 精神医学, 59; 1037-1044, 2017
9) 糸川昌成: バイオマーカー発展の長期展望. 精神科, 30; 217-220, 2017
10) Itokawa, M., Miyashita, M., Arai, M., et al.: Pyridoxamine: a novel treatment for schizophrenia with enhanced carbonyl stress. Psychiatry Clin Neurosci, 72; 35-44, 2018![]()
11) Katsuta, N., Ohnuma, T., Maeshima, H., et al.: Significance of measurements of peripheral carbonyl stress markers in a cross-sectional and longitudinal study in patients with acute-stage schizophrenia. Schizophr Bull, 40; 1366-1373, 2014![]()
12) Koyama, Y., Takeishi, Y., Arimoto, T., et al.: High serum level of pentosidine, an advanced glycation end product (AGE), is a risk factor of patients with heart failure. J Card Fail, 13; 199-206, 2007![]()
13) Lerner, V., Kaptsan, A., Miodownik, C., et al.: Vitamin B6 in treatment of tardive dyskinesia: a preliminary case series study. Clin Neuropharmacol, 22; 241-243, 1999![]()
14) Lerner, V., Miodownik, C., Kaptsan, A., et al.: Vitamin B6 as add-on treatment in chronic schizophrenic and schizoaffective patients: a double-blind, placebo-controlled study. J Clin Psychiatry, 63; 54-58, 2002![]()
15) Levine, J., Stahl, Z., Sela, B. A., et al.: Homocysteine-reducing strategies improve symptoms in chronic schizophrenic patients with hyperhomocysteinemia. Biol Psychiatry, 60; 265-269, 2006![]()
16) Lewis, S. W., Barnes, T. R., Davies, L., et al.: Randomized controlled trial of effect of prescription of clozapine versus other second-generation antipsychotic drugs in resistant schizophrenia. Schizophr Bull, 32; 715-723, 2006![]()
17) Makita, Z., Radoff, S., Rayfield, E. J., et al.: Advanced glycosylation end products in patients with diabetic nephropathy. N Engl J Med, 325; 836-842, 1991![]()
18) McEvoy, J. P., Lieberman, J. A., Stroup, T. S., et al.: Effectiveness of clozapine versus olanzapine, quetiapine, and risperidone in patients with chronic schizophrenia who did not respond to prior atypical antipsychotic treatment. Am J Psychiatry, 163; 600-610, 2006![]()
19) Miyashita, M., Arai, M., Yuzawa, H., et al.: Replication of enhanced carbonyl stress in a subpopulation of schizophrenia. Psychiatry Clin Neurosci, 68; 83-84, 2014![]()
20) Miyashita, M., Arai, M., Kobori, A., et al.: Clinical features of schizophrenia with enhanced carbonyl stress. Schizophr Bull, 40; 1040-1046, 2014![]()
21) Miyata, T., Taneda, S., Kawai, R., et al.: Identification of pentosidine as a native structure for advanced glycation end products in beta-2-microglobulin-containing amyloid fibrils in patients with dialysis-related amyloidosis. Proc Natl Acad Sci U S A, 93; 2353-2358, 1996![]()
22) Miyata, T., van Ypersele de Strihou, C., Kurokawa, K., et al.: Alterations in nonenzymatic biochemistry in uremia: origin and significance of “carbonyl stress” in long-term uremic complications. Kidney Int, 55; 389-399, 1999![]()
23) Olfson, M., Gerhard, T., Huang, C., et al.: Premature mortality among adults with schizophrenia in the United States. JAMA Psychiatry, 72; 1172-1181, 2015![]()
24) Park, L., Raman, K. G., Lee, K. J., et al.: Suppression of accelerated diabetic atherosclerosis by the soluble receptor for advanced glycation endproducts. Nat Med, 4; 1025-1031, 1998![]()
25) Sandyk, R., Pardeshi, R.: Pyridoxine improves drug-induced parkinsonism and psychosis in a schizophrenic patient. Int J Neurosci, 52; 225-232, 1990![]()
26) Schaumburg, H., Kaplan, J., Windebank, A., et al.: Sensory neuropathy from pyridoxine abuse. A new megavitamin syndrome. N Engl J Med, 309; 445-448, 1983![]()
27) Tiihonen, J., Lönnqvist, J., Wahlbeck, K., et al.: 11-year follow-up of mortality in patients with schizophrenia:a population-based cohort study (FIN11 study). Lancet, 374; 620-627, 2009![]()
28) Yoo, D. Y., Kim, W., Kim, D. W., et al.: Pyridoxine enhances cell proliferation and neuroblast differentiation by upregulating the GABAergic system in the mouse dentate gyrus. Neurochem Res, 36; 713-721, 2011![]()
29) Yoo, D. Y., Kim, W., Nam, S. M., et al.: Chronic effects of pyridoxine in the gerbil hippocampal CA1 region after transient forebrain ischemia. Neurochem Res, 37; 1011-1018, 2012![]()