クロザピンは治療抵抗性統合失調症の治療において有用であるが,一方で重篤な副作用である無顆粒球症を引き起こす.そこでわれわれはクロザピン誘発性無顆粒球症に関連する遺伝的因子の同定を目的とし研究を行った.まず,日本人のクロザピン誘発性無顆粒球症患者と顆粒球減少症患者を合わせた無顆粒球症・顆粒球減少症患者群50人と日本人健常対照者群2,905人について全ゲノムSNP解析を行った.その結果,有意水準を下回るP値を示すSNPが4つ同定され,すべてが6番染色体のHLA領域に位置していた(rs1800625,P=3.46×10-9,オッズ比=3.8).そのため続いて,無顆粒球症・顆粒球減少症患者群50人と日本人健常対照者群1,891人を用いてHLA関連解析を行った.HLA関連解析ではHLA-B*59:01に有意な関連を認めた(P=3.81×10-8,オッズ比=10.7).次にHLA-B*59:01を予測因子として用いて,顆粒球減少症患者群へのクロザピン再投与の可能性を検討した.顆粒球減少症患者群はクロザピン投与を続けた場合に,無顆粒球症へ進展する「潜在的な無顆粒球症患者群」と,無顆粒球症へ進展しない可能性の高い「非無顆粒球症患者群」の2つの群からなる混合集団であるというモデルを想定し,顆粒球減少症患者群のなかの「非無顆粒球症患者群」の割合を推計した.その結果,顆粒球減少症患者群のなかでは,約50%が「非無顆粒球症患者群」であった.さらに顆粒球減少症患者群におけるHLA-B*59:01を用いた検査での「非無顆粒球症患者群」の陽性的中率は約60%であり,再投与した場合は約60%が無顆粒球症に進展しないと推計できた.これらの結果より,顆粒球減少症患者群においても,一部の患者に対しては,クロザピンの再投与は絶対的な禁忌ではない可能性があることが示された.
はじめに
治療抵抗性統合失調症は「複数の抗精神病薬」を「十分な量」 「十分期間」服用しても「改善が認められない」ことによって定義され,統合失調症患者全体の3分の1にあたると報告されている.クロザピンはその治療抵抗性統合失調症において適応が認められている唯一の薬剤であり,その反応率は60~70%とされる4).このように治療抵抗性統合失調症治療において,有用な薬剤であるのにもかかわらず,世界的にも,また本邦でもクロザピンは十分に普及しているとはいえない.普及しない大きな理由には,クロザピン誘発性無顆粒球症という重篤な副作用が約1%の頻度で起きてしまうことがあると考えられる.無顆粒球症は血液中の好中球数が500個/mm3未満となり,感染症に対する抵抗力が下がる病態で,その死亡率は2~4%程度である6).そのため副作用の早期発見・早期対処などを目的とし,定期的血液検査の確実な実施と処方の判断を支援するしくみとしてクロザリル患者モニタリングサービス(CPMS)があり,その運用手順に則りクロザピンの治療は行われる.具体的には好中球数や白血球数の減少を早期に発見するため,頻回の血液検査を行いモニタリング(白血球数・好中球数のモニタリング頻度は,特に問題がなければ最初の26週間は1週間に1回,その後は最大で2週間に1回まで間隔を空けることができるが,モニタリングの継続は必要である)を行うわけであるが,患者にとって大きくはないが侵襲的であり,ストレスフルであり,そして医療者にとっても一定の手間がかかる.また,治療開始時には入院が必要であり,血液内科との連携が必要であるなど,そもそも使用できる環境にある施設は限られる.加えて,心理的要因なのかもしれないが,「無顆粒球症に対する恐れ」を患者のみならず精神科医ももつことなどが普及しにくい要因になっていると考えられる.
治療を行ううえで最も回避したい病態である無顆粒球症の診断基準は,上述のように好中球数500個/mm3未満である.しかし実際の臨床では,安全性に配慮して顆粒球減少症(好中球数1,500個/mm3未満)もしくは白血球減少症(白血球数3,000個/mm3未満)となった時点でCPMSの運用手順に則り,クロザピンの投与を中止しなければならない.そして,基準値をわずかに下回った場合においても,投与を中止せねばならず,たとえ速やかに血球数が回復したとしても,またクロザピンが著効していた症例でも再投与をすることはできない.一方で,白血球数・好中球数が比較的容易に変動することを医師は経験している.クロザピンを処方し,頻回に血球数をモニタリングするようになると,ますますそれを実感することが多いであろう.
現時点では,一旦顆粒球減少症や白血球減少症に陥った症例が,そのまま無顆粒球症まで進展するのか,それとも速やかに回復するものなのかを見分けることができないため,安全に使用するために,顆粒球減少症や白血球減少症に陥った時点で投与を中止するという制約は,やむを得ないことである.そこには安全性の担保と,この制約のために本来は無顆粒球症への進展の危険性が低い(と臨床的・直感的に考える)患者までもが有用な薬剤を使用できなくなってしまうことのジレンマが存在する.
もし,クロザピン誘発性無顆粒球症発症のリスクとなる遺伝的因子が同定され発症の危険性を推定できるようになれば,危険性が低い患者についてはよりクロザピン治療が導入しやすくなり,より多くの治療抵抗性統合失調症患者が投与を受けることができる可能性がある.また,一旦投与が中止された患者でも,無顆粒球症に進展する危険性の低い患者を見分けて再投与をすることができるようになれば,その患者はクロザピンの投与を続けることができる.一方で危険性の高い患者については,慎重な投与やモニタリングを行うことで,無顆粒球症の発症を減らすことができる可能性がある.このことはクロザピンの代替薬がない現状において,治療抵抗性統合失調症患者にとって大きなメリットになると考えられる.
I.クロザピン誘発性無顆粒球症の薬理ゲノム学研究
薬理ゲノム学は,薬物の反応性や副作用に関連する遺伝子を同定することを目的とした研究である.同定した遺伝子が,大きな効果量をもつ場合はゲノムバイオマーカーとして,薬物の有効性の予測,副作用発症の予測と未然防止,用量の設定などに役立ち,オーダーメード医療につながる可能性をもつ.そのため多くの薬物の副作用,治療反応性に関して研究がなされてきた.クロザピン誘発性無顆粒症に関連する遺伝的因子の探索の歴史は,1990年まで遡る.無顆粒球症発症の機序が免疫を介したものであると予測されていたことや,それまでに他の薬剤の重症な副作用において,主要組織適合遺伝子複合体(major histocompatibility complex:MHC)領域にあるヒト白血球型抗原(human leukocyte antigen:HLA)遺伝子との関連が明らかになっていたことなどから,HLA遺伝子をターゲットとした研究が行われ,関連が複数報告された.しかし,それらの結果の多くは,追試による再現性は乏しいものであった2)6).そのなかで,最も有望なものは2011年にAthanasiou, M. C.らが報告した一塩基多型(single nucleotide polymorphism:SNP)HLA-DQB1 6672G>Cである.この研究では,主に白人を対象として,2つの独立したサンプルセットを用いて関連が確認され,オッズ比(OR)が16.9(P<0.001)と大きな効果量をもつものであった1).
近年ではゲノムワイドな解析を用いた遺伝子同定が行われるようになり,2014年Goldstein, J. I.らは白人を対象とした研究で,クロザピン誘発性無顆粒球症・顆粒球減少症(無顆粒球症と顆粒球減少症を合わせた群:好中球数<1,000個/mm3)とHLA-DQB1(126Q)(OR=0.19,P=4.7×10-14)とHLA-B(158T)(OR=3.3,P=6.4×10-10)の2つのSNPが関連することを明らかにした3).
このように無顆粒球症の遺伝的リスクの同定は白人を対象とした研究が先行していたが,HLA遺伝子は人種によって多型の頻度が異なるため,白人での結果を日本人にそのままあてはめることはできない.そのため日本人における独自の無顆粒球症の遺伝的リスクの同定が望まれていた.そこでわれわれは,日本人のクロザピン誘発性無顆粒球症の遺伝的リスク同定をめざした薬理ゲノム学研究を行った.
II.日本人のクロザピン誘発性無顆粒球症の薬理ゲノム学研究
1.クロザピン誘発性無顆粒球症・顆粒球減少症に関連する遺伝的因子の同定
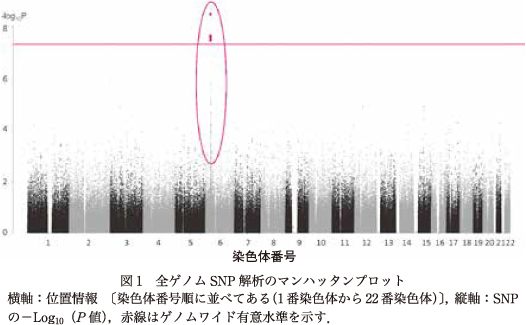
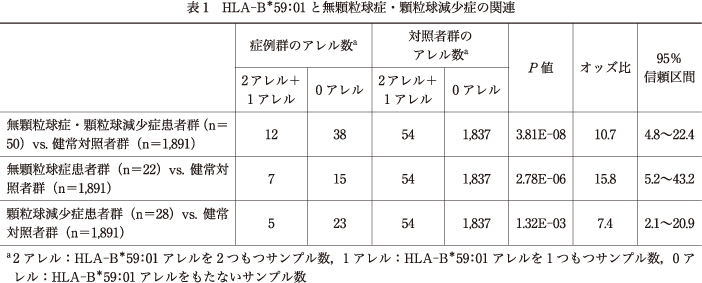
われわれはクロザピン誘発性無顆粒球症・顆粒球減少症の発症に関連する遺伝的因子を同定するために,まず,日本人のクロザピン誘発性無顆粒球症患者と顆粒球減少症患者を合わせた無顆粒球症・顆粒球減少症患者群50人と日本人健常対照者群2,905人について全ゲノムSNP解析を行った.その結果,有意水準を下回るP値を示すSNPが4つ同定され,すべてが6番染色体のHLA領域に位置していた(rs1800625,P=3.46×10-9,OR=3.8)(図1).そのため,HLA遺伝子のどの多型がクロザピン誘発性無顆粒球症・顆粒球減少症と関連しているかを同定するため,無顆粒球症・顆粒球減少症患者群50人と日本人健常対照者群1,891人を用いて,HLA遺伝子のHLA-A,HLA-C,HLA-B,HLA-DRB1のジェノタイピングとHLA関連解析を行った.HLA関連解析の結果,HLA-B*59:01に有意な関連を認めた(P=3.81×10-8,OR=10.7)(表1)5).
2.HLA-B*59:01の臨床における有用性の検討
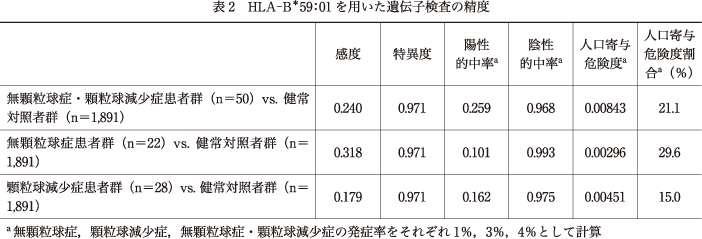
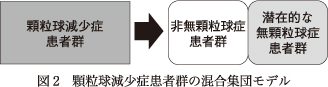
次にHLA-B*59:01の無顆粒球症・顆粒球減少症の発症予測因子としての有用性を検討した.まず,クロザピン導入前に発症を予測する事前の遺伝子検査の有用性を検討した.HLA-B*59:01は事前の遺伝子検査においては,感度が低いことから陽性的中率も低く,そのままでは臨床に用いることは難しいことがわかった(表2).そこで次に,HLA-B*59:01を予測因子として用いて,顆粒球減少症患者群へのクロザピン再投与の可能性を検討した.顆粒球減少症患者群と無顆粒球症患者群を分けてHLA-B*59:01との関連を検討すると,無顆粒球症に対する効果量のほうが顆粒球減少症に対する効果量よりも2倍程度大きいことがわかった(表1).この結果より,顆粒球減少症患者群はクロザピン投与を続けた場合に,無顆粒球症へ進展する「潜在的な無顆粒球症患者群」と,無顆粒球症へ進展しない可能性の高い「非無顆粒球症患者群」という互いに連続性のない2つの群からなる混合集団であるというモデルを想定した(図2).このモデルのもとで,無顆粒球症患者群と対照者群のHLA-B*59:01の保有率を用いることで,顆粒球減少症患者群のなかに「非無顆粒球症患者群」がどの程度の割合で存在するのかを一次方程式を用いて推計することができる.その結果,顆粒球減少症患者群のなかでは,約50%が無顆粒球症に進展しない可能性の高い「非無顆粒球症患者群」であった.さらに,HLA-B*59:01を保有しない顆粒球減少症患者群のなかでは約60%が「非無顆粒球症患者群」であることがわかった.すなわち,顆粒球減少症患者群においてHLA-B*59:01を用いた,「非無顆粒球症患者群」の陽性的中率は約60%であり,再投与した場合は約60%が無顆粒球症に進展しないと推計できた5).この結果は,臨床医が経験上直感で感じとっていた,好中球減少を起こし顆粒球減少症には至ったが,無顆粒球症には陥らない「偽物」(非無顆粒球症患者群)が存在するということを,科学的にデータを用いて示したものである.そしてこのことから,顆粒球減少症患者群においても,一部の患者に対してはクロザピンの再投与は,理論上絶対的な禁忌ではないことが示唆されたのである.しかし,実際の臨床判断に用いるには,再投与時の成功率はさらに高いものが求められるであろう.
おわりに
本研究により日本人のクロザピン誘発性無顆粒球症・顆粒球減少症の遺伝的リスクとしてHLA-B*59:01が同定された.HLA-B*59:01はクロザピン導入前の事前の発症予測においては,感度が低いことから陽性的中率も低く,すぐに臨床応用することはできない.しかし顆粒球減少症患者における再投与での臨床判断に用いることができる可能性や,クロザピンの投与基準を科学的に定める1つの判断材料になる可能性があると考える.今後クロザピン誘発性無顆粒球症の薬理ゲノム学研究が進み,今まで同定されてきた遺伝的リスクの追試がなされるとともに,新たな遺伝的リスクが同定され,それらの遺伝的リスクを組み合わせた精度の高い検査法が構築されれば,臨床に用いることができる可能性がある.そのことによりクロザピンがより使用しやすいものになれば,今現在症状の改善を得られないばかりか,薬剤が多剤大量となり,それに伴う副作用を被る危険性にさらされている治療抵抗性統合失調症患者に大きな利益をもたらすと考えられる.
なお,本論文に関連して開示すべき利益相反はない.
謝 辞 本稿で報告した受賞論文の研究は藤田保健衛生大学,大阪大学,理化学研究所をはじめ,全国の精神科病院や大学が参加する日本クロザピン薬理ゲノム学コンソーシアム(Clozapine Pharmacogenomics Consortium of Japan:CPC-J)と共同で行ったものです.CPC-Jに参画された先生方はもちろん,CPC-Jをオーガナイズしていただき,責任著者になっていただいた大阪大学の橋本亮太先生,タイピングや統計解析などにご指導いただいた理化学研究所の筵田泰誠先生,モデル化にご指導いただいた藤田保健衛生大学衛生学の橋本修二先生,そして上司の岩田仲生先生に感謝申し上げます.
なお,受賞対象となった論文は2報である.今回は,特に「クロザピン誘発性無顆粒球症・顆粒球減少症の薬理ゲノム学研究(Pharmacogenomic Study of Clozapine-Induced Agranulocytosis/Granulocytopenia in a Japanese Population)」について報告した.
1) Athanasiou, M. C., Dettling, M., Cascorbi, I., et al.: Candidate gene analysis identifies a polymorphism in HLA-DQB1 associated with clozapine-induced agranulocytosis. J Clin Psychiatry, 72 (4); 458-463, 2011![]()
2) de With, S. A. J., Pulit, S. L., Staal, W. G., et al.: More than 25 years of genetic studies of clozapine-induced agranulocytosis. Pharmacogenomics J, 17 (4); 304-311, 2017![]()
3) Goldstein, J. I., Jarskog, L. F., Hilliard, C., et al.: Clozapine-induced agranulocytosis is associated with rare HLA-DQB1 and HLA-B alleles. Nat Commun, 5; 4757, 2014![]()
4) Lally, J., Gaughran, F., Timms, P., et al.: Treatment-resistant schizophrenia: current insights on the pharmacogenomics of antipsychotics. Pharmgenomics Pers Med, 9; 117-129, 2016![]()
5) Saito, T., Ikeda, M., Mushiroda, T., et al.: Pharmacogenomic Study of Clozapine-Induced Agranulocytosis/Granulocytopenia in a Japanese Population. Biol Psychiatry, 80 (8); 636-642, 2016![]()
6) Verbelen, M., Lewis, C. M.: How close are we to a pharmacogenomic test for clozapine-induced agranulocytosis? Pharmacogenomics, 16 (9); 915-917, 2015![]()